1일 메지온에 따르면 이 회사는 신약후보물질 유데나필을 이용해 미국 캐나다 한국 등에서 임상 3상을 진행 중이다. 지난 6월 400명 규모의 환자 모집을 완료했다. 약 6개월의 추적관찰 기간을 감안하면 연내 임상시험이 마무리되고, 내년 1분기에는 주요 결과가 공개될 것으로 보고 있다.
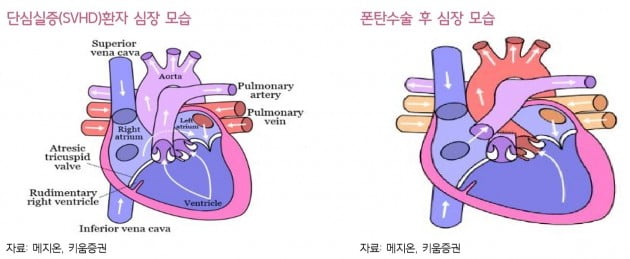
폰탄수술은 선천성 심장기형 중 하나인 단심실 환자들에게 시행하는 수술이다. 그러나 20세가 넘어가면 호흡 기능이 급속도로 떨어지면서 만성심부전증 간경화 간암 등 여러 합병증으로 환자 대부분이 사망에 이르게 된다. 유데나필은 앞선 임상에서 경쟁 물질 대비 심각한 부작용 없이, 심장 기능 및 운동능력을 향상시켰다.
여기에 판매허가를 받게 되면 우선심사권(PRV)도 획득하게 된다. PRV는 열대성 및 희귀질환 신약개발을 촉진하기 위해 미 식품의약국(FDA)가 만든 제도다. 신약 승인 검토기간을 6개월로 단축해 준다. 다른 기업에게 판매도 가능하다.
정승규 키움증권 연구원은 "현재까지 23개의 신약에 대해 PRV가 발급됐으며, 평균 거래금액은 약 1700억원 수준"이라며 "메지온 역시 희귀질환인 폰탄수술 치료제를 개발하고 있기 때문에 메지온의 기업가치를 산정할 때 PRV 가치를 감안하는 것이 합리적"이라고 말했다.
한민수 한경닷컴 기자 hms@hankyung.com