류영진 식품의약품안전처장은 27일 서울 태평로2가 더플라자호텔에서 ‘제약업계 최고경영자(CEO) 간담회’를 열고 공동 생동시험 참여 기업을 최대 4곳으로 제한한다고 발표했다. 유예기간을 거쳐 내년 7월부터 시행하고 3년 뒤엔 완전 폐지하기로 했다.
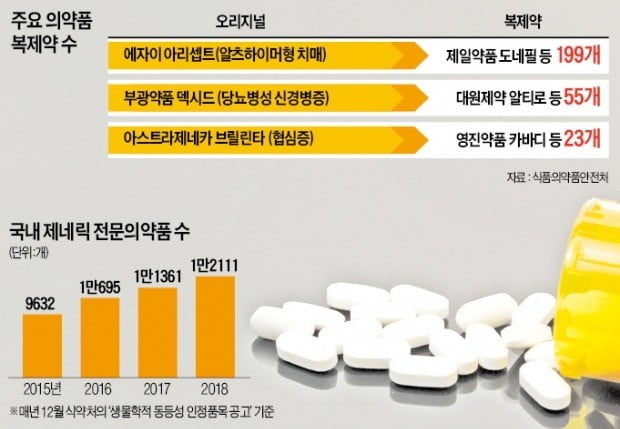
생동시험은 오리지널 약과 같은 약효 등을 갖고 있는지 검증하는 절차다. 제네릭 허가에 필수적이다. 한 제약사가 주도해 생동시험을 하면 여러 제약사가 위탁 방식으로 참여해 비용을 분담한다. 오리지널 약의 특허가 풀리면 한꺼번에 수십 종의 제네릭이 쏟아지는 배경이기도 하다. 일본 에자이의 알츠하이머 치매 치료제 아리셉트 특허가 2008년 풀리자 199개의 제네릭이 출시됐다. 지난해 상반기 기준 생동시험 건당 7.5개의 제네릭이 허가를 받았다.
해외에는 없는 이 제도는 국내 제약산업 활성화를 명분으로 2003년 도입됐다. 하지만 지난해 고혈압약에 발암 물질이 포함돼 논란이 벌어졌던 ‘발사르탄 사태’가 터지면서 무분별한 제네릭 규제 필요성이 제기됐다. 당시 국내에서 회수된 발사르탄 복제약은 115개에 달했다.
식약처는 곧바로 제도 개선 작업에 나서기로 했다. 다음달 관련 행정예고를 한 뒤 의견 수렴을 거쳐 상반기 중에 관련 규정 개정을 마무리짓겠다는 계획이다. 식약처 관계자는 “이번 조치가 국내 제약사에서 개발한 복제약의 수출 경쟁력을 강화하고 연구개발(R&D) 중심으로의 기업 체질 변화 등에도 기여할 것”이라고 말했다.
중소 제약사 구조조정 신호탄
제약사들은 희비가 엇갈린다. 자금 여력이 있는 대형 제약사는 환영하는 분위기다. 경쟁자가 줄어 반사이익을 볼 것이라는 분석도 나온다. 한 대형 제약사 관계자는 “비슷한 약이 쏟아져 나오면서 기술력보다는 리베이트와 영업력으로 승부하는 나쁜 관행이 개선될 수 있을 것으로 본다”고 말했다.
중소 제약사들은 비상이 걸렸다. 개발비 부담이 커지기 때문이다. 생동시험에는 건당 1억~5억원가량이 들어간다. 조용준 한국제약협동조합 이사장(동구바이오제약 대표)은 “제약산업 품질 경쟁력이 높아지는 등 긍정적 측면도 있지만 자금 여력이 없는 중소 제약사는 제품 개발에 어려움을 겪게 될 것”이라고 했다.
제약산업의 고질적인 과당 경쟁이 해소될 것이라는 분석도 있다. 정윤택 제약산업전략연구원장은 “이번 조치로 의약품 안전관리는 물론 과당 경쟁 억제 등으로 리베이트가 줄어드는 효과가 기대된다”며 “공동 생동시험 기업끼리 가격 짬짜미를 하던 관행도 없어져 참여 기업이 줄어들더라도 약가 인하 측면에서 긍정적”이라고 했다. 이어 “R&D 역량을 지닌 기업의 시장 진입을 촉진하기 위해 일찍 진입하는 기업에 이익을 주는 ‘계단식 약가 제도’ 부활 등 후속 조치를 검토해야 한다”고 덧붙였다.
■생물학적 동등성 시험
시험 대상 의약품이 인체에서 오리지널 의약품과 같은 작용을 하는지 검증하는 절차. 제네릭을 판매하려면 이 절차를 반드시 거쳐야 한다.
양병훈 기자 hun@hankyung.com