오세중 연구원은 "리보세라닙 위암 임상 3상에서 1차 유효성 지표인 전체생존기간(OS)의 유의성을 증명하지 못했기에 허가는 불가능할 것"이라며 "위암 2차 치료제, 간암 1차 치료제로서의 가능성도 기대치를 낮출 필요가 있다"고 말했다.
간암과 위암 2차 치료제는 임상 진행 후 실제 허가까지 긴 시간이 필요하기 때문이다. 리보세라닙과 면역관문억제제 캄렐리주맙의 병용 임상 3상은 간암 1차 치료제로 이제 시작됐고, 위암 2차 치료제로 파클리탁셀과의 병용 1·2상이 진행되고 있다는 것이다.
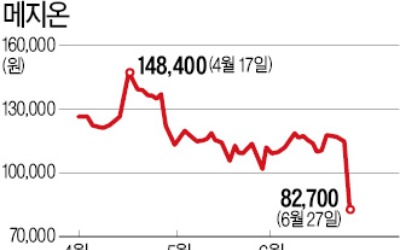
이번 결과로 제약바이오 업종에 대한 투자심리는 나빠질 것으로 봤다. 오 연구원은 "메지온과 헬릭스미스의 임상 3상 결과, 신라젠 무용성 평가가 모두 확인되기 전까지는 투자심리 개선이 어려울 것"이라며 "임상 결과를 기반으로 성과 기술료(마일스톤)가 예상되는 기업에 대한 선별적 접근이 필요하다"고 했다.
한민수 한경닷컴 기자 hms@hankyung.com