샤페론, 유럽서 코로나 치료제 임상 2상 승인
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
국내기업 중 유럽임상 가장 빨라
루마니아서 환자 60명 대상
루마니아서 환자 60명 대상
샤페론은 유럽의약품감독국(EMA)으로부터 항염증 치료 신약 후보물질인 ‘누세핀’을 코로나19로 인한 폐렴 환자에게 투여하는 임상 2상을 승인받았다고 23일 밝혔다. 이 회사는 루마니아 병원 네 곳에서 코로나19로 인한 폐렴 환자 60명을 대상으로 임상을 한다. 이르면 이달 말 첫 환자에게 약물을 투여하고 올해 말께 임상을 종료한다. 회사 관계자는 “임상 2상 결과가 좋으면 대형 제약사 등에 기술이전을 통해 내년 임상 3상에 나설 계획”이라고 했다.
누세핀은 면역세포에 있는 염증 유발물질을 억제하면서 동시에 체내 염증억제세포 수를 증가시켜 사이토카인 폭풍을 억제하는 신약 후보물질이다. 사이토카인 폭풍은 바이러스에 대해 면역체계가 과도하게 반응해 장기 등에 염증을 일으키는 증상이다. 코로나19 치명률을 높이는 주요 원인이다.
누세핀은 한두 개 염증유발 인자를 차단하는 기존 치료제와 다르다. 회사 관계자는 “누세핀은 인터루킨(IL)-1베타, IL-18 등 4개 이상의 염증 인자를 동시에 차단하는 데다가 스테로이드계 약물에서 나타나는 부작용 우려도 없다”고 했다.
샤페론은 나노바디 항체를 이용한 코로나19 치료제 개발도 추진 중이다. 나노바디 항체는 기존 항체 대비 크기가 10분의 1 수준에 불과해 병변 조직에 침투하기가 용이하다. 회사 관계자는 “사용이 간편하도록 흡입형 치료제로 개발하겠다”고 말했다.
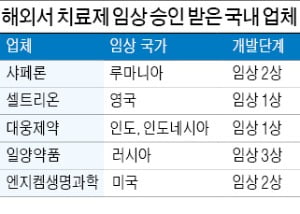
다른 국내 업체들도 유럽 등에서 임상시험에 나서고 있다. 셀트리온은 지난달 영국에서 임상 1상 승인을 받았다. 약물의 안전성을 확인하는 대로 임상 2·3상에 나서 연말께는 임상 중간 결과를 확보한다는 계획이다.
미국 아시아 등에서도 속속 임상에 뛰어들고 있다. 엔지켐생명과학은 미국 식품의약국(FDA)으로부터 지난 6일 임상 2상 승인을 받고 이르면 내년 상반기께 임상을 마무리할 계획이다. 일양약품은 러시아 정부의 허가를 받아 현지에서 백혈병 치료제 슈펙트로 코로나19 치료제 임상 3상에 들어갔다. 대웅제약은 구충제 성분인 니클로사마이드를 코로나19 치료제로 개발하는 임상 1상을 인도에서 승인받았다.
이주현 기자 deep@hankyung.com
![정부 "전공의, 코로나19 진료 참여"…대전협, 진료·협상 병행[종합]](https://img.hankyung.com/photo/202008/01.23575348.3.jpg)
![[속보] 전공의협의회, 코로나19 대응 위한 진료 적극 참여키로](https://img.hankyung.com/photo/202008/01.23575287.3.jpg)

![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


