케이캡정은 지난해 미란성 위식도역류질환에 대한 임상 3상 연구에 이어 논문까지 국제학술지에 실리면서, 새로운 계열의 위식도역류질환 신약으로 유효성과 안전성을 인정받았다는 설명이다.
AP&T에는 위궤양 환자에서 'P-CAB' 계열 신약 케이캡정(성분명 테고프라잔)과 'PPI' 계열의 란소프라졸 성분 제품 간 유효성과 안전성을 비교한 임상 3상 결과가 실렸다.
이번 임상은 국내 다기관에서 위궤양을 진단받은 306명의 환자를 이중눈가림으로 무작위 배정해 케이캡정 50mg(102명)과 케이캡정 100mg(102명), 그리고 란소프라졸 30mg(102명) 투여군으로 나눠 8주간 진행됐다.
임상 결과, 위궤양 치료 효과 및 안전성에 있어 케이캡정 50mg과 100mg은 란소프라졸 30mg 대비 비열등함을 보였다.
HK이노엔 관계자는 "이번 논문 등재를 통해 P-CAB 계열 위식도역류질환 신약 케이캡정의 유효성과 안전성을 세계적으로 인정받았다"며 "적응증 확대 노력과 더불어 차별화 연구를 지속해, 세계 무대에서 활약하는 대한민국 신약으로 키울 것"이라고 말했다.
케이캡정은 지난해 국내에서 출시됐다. 미란성 및 비미란성 위식도역류질환, 위궤양 치료에 이어 헬리코박터파일로리 제균 요법까지 네 개의 적응증을 갖고 있다.
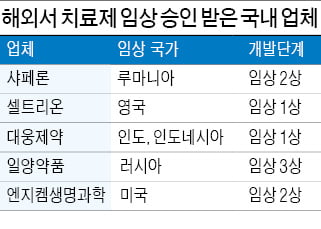
기존 PPI(프로톤 펌프 억제제) 제제 대비 약효가 빠르게 나타나고, 식전·식후 상관없이 복용이 가능하다. 또 우수한 약효 지속력으로 야간 위산 분비를 억제하는 점 등에서 위식도역류질환 치료제 시장에서 영역을 넓히고 있다고 회사 측은 전했다. 올 들어 7월까지 원외처방데이터 유비스트 기준 374억원을 기록했다. 국내 및 중국, 동남아시아, 중남미 국가 등 총 23개 국가에 진출해있고, 최근에는 미국에서 임상 1상을 승인받았다.
한민수 기자 hms@hankyung.com