"백신 원료 속 균이 사망원인 일수도"…식약처 "원인분석 중"
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
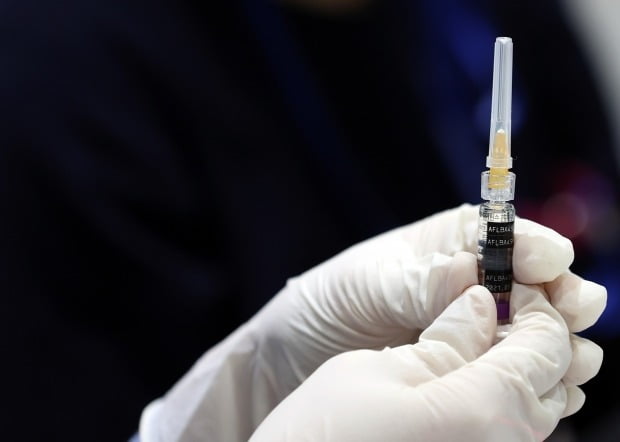
국회 보건복지위 국감장서 쟁점된 독감 백신

보건 당국은 이과 관련해 독감 백신의 제조와 출하에 이르기까지 이중·삼중으로 관리하고 있다고 반박한 뒤 현재 원인을 분석 중인만큼 결과가 나오는 대로 공개하겠다고 밝혔다. 아울러 독감 백신 제조업체에서는 철저한 무균 상태에서 백신의 제조가 이뤄지고 검증을 받는 만큼 독성이나 균이 있다는 지적은 받아들이기 어렵다는 입장을 보였다.
국회 보건복지위원회 소속 강기윤 국민의힘 의원은 22일 열린 국정감사에서 충남대학교 수의학과 서상희 교수에게 독감 백신 사망사고의 원인에 대해 자문한 결과를 공개했다.
강기윤 의원은 "독감 바이러스를 유정란에 넣어 배양할 때 톡신이나 균이 기준치 이상 존재할 경우 사망에 이르게 하는 쇼크를 유발할 수 있다는 사실을 확인했다"고 밝혔다.
독감 백신 접종 후 드물게 나타날 수 있는 중증 이상 반응에는 감염에 의한 신경계 질환인 '길랭-바레 증후군'과 중증 알레르기 반응인 '아나필락시스 쇼크' 등이 있다. 이때 유정란의 톡신이나 균이 접종자의 면역체계에 영향을 미치면서 자신을 공격하거나 그 자체로 알레르기 반응을 일으킬 수 있다는 게 강기윤 의원의 주장이다.
강기윤 의원은 또 세포로 독감 바이러스를 배양할 때에도 '배지'에서 균 등이 자랄 수 있다고 봤다. 국내에서 독감 백신을 생산하는 방식은 바이러스를 배양하는 방법에 따라 유정란 배양과 세포 배양으로 나뉘는데, 두 가지 방식 모두 문제가 될 수 있다는 것이다.
아울러 식품의약품안전처가 백신의 출하를 승인할 때 일부 물량에 대해서만 무균 검사와 톡신 검사를 샘플링 방식으로 실시하고 있다고 지적했다. 또 백신 제조사의 생산 과정이나 유통·접종 이전 백신의 균과 톡신 상태는 따로 점검하지 않고 있다고 주장했다.
이의경 식약처장은 "백신 제조·생산·품질관리 등 모든 공정을 철저하게 관리하고 있고 유정란 생산시설도 정기 점검해 문제가 없도록 하고 있다"고 답했다.
이어 "제조 공정에서도 무균 여과와 정제 과정을 거치고, 이후 다른 제품과 달리 식약처의 국가 출하승인을 거친다"며 "그 과정에서 무균 검사와 엔도톡신(균체 내 독소 시험) 검사를 무작위 채취 방식으로 진행해 이중삼중으로 관리하고 있다"고 강조했다.
조준혁 한경닷컴 기자 presscho@hankyung.com

![경남서 독감 백신 접종 오늘 하루에만 3명 잇따라 사망 [종합]](https://img.hankyung.com/photo/202010/01.24160367.3.jpg)


![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


