존슨앤드존슨-얀센, 화이자에 이어 코로나19 백신 사전검토 착수
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
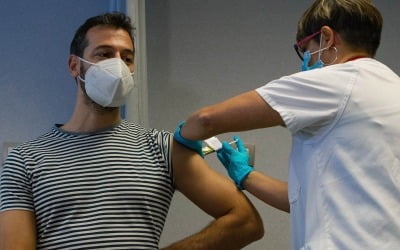
22일 존슨앤드존스·얀센이 신종 코로나바이러스 감염증(코로나19) 백신의 사전검토를 신청했다. 식품의약품안전처가 사전검토하고 있는 코로나19 백신은 이로써 세 개다.
사전검토는 백신 개발업체가 허가신청 전 품질, 비임상, 임상 등의 자료를 미리 검토받을 수 있도록 한 제도로, 허가신청 이후 심사에 걸리는 시간을 단축시킬 수 있다. 아스트라제네카는 지난 10월 6일 비임상 자료에 대한 사전검토를 신청했으며, 화이자는 18일 비임상, 1상·2상·3상에 대한 사전검토를 신청했다.
존슨앤드존슨이 소유한 제약업체인 얀센의 백신은 정부에서 400만 명분의 백신을 도입하기로 발표한 백신이다. 이번에 비임상, 품질 자료에 대한 사전검토를 신청했다. 해당 백신은 내년 1월 미국 식품의약국(FDA)에 긴급사용 승인을 요청할 예정인 것으로 알려졌다.
얀센의 백신은 아스트라제네카와 동일한 방식인 '바이러스벡터' 백신을 개발하고 있다. 아데노바이러스를 운반체로 이용하며, 1회만 접종하면 된다. 이에 따라 허가전담심사팀인 '바이러스벡터 백신팀'에서 해당 백신의 독성, 약리 및 품질자료를 사전에 검토할 예정이다.
최지원 기자 jwchoi@hankyung.com
사전검토는 백신 개발업체가 허가신청 전 품질, 비임상, 임상 등의 자료를 미리 검토받을 수 있도록 한 제도로, 허가신청 이후 심사에 걸리는 시간을 단축시킬 수 있다. 아스트라제네카는 지난 10월 6일 비임상 자료에 대한 사전검토를 신청했으며, 화이자는 18일 비임상, 1상·2상·3상에 대한 사전검토를 신청했다.
존슨앤드존슨이 소유한 제약업체인 얀센의 백신은 정부에서 400만 명분의 백신을 도입하기로 발표한 백신이다. 이번에 비임상, 품질 자료에 대한 사전검토를 신청했다. 해당 백신은 내년 1월 미국 식품의약국(FDA)에 긴급사용 승인을 요청할 예정인 것으로 알려졌다.
얀센의 백신은 아스트라제네카와 동일한 방식인 '바이러스벡터' 백신을 개발하고 있다. 아데노바이러스를 운반체로 이용하며, 1회만 접종하면 된다. 이에 따라 허가전담심사팀인 '바이러스벡터 백신팀'에서 해당 백신의 독성, 약리 및 품질자료를 사전에 검토할 예정이다.
최지원 기자 jwchoi@hankyung.com


![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


