올리패스 "非마약성 진통제 내년초 기술수출"
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
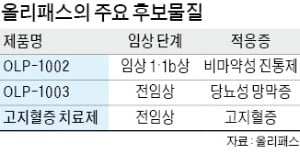
RNA 기반 신약 'OLP-1002'
세포투과성 높아 적은 양도 효과
당뇨성 망막증 신약 내년 전임상
7년내 美 FDA 판매 허가 목표
세포투과성 높아 적은 양도 효과
당뇨성 망막증 신약 내년 전임상
7년내 美 FDA 판매 허가 목표

임상1상서 효능까지 확인
2018년 말 영국 임상을 시작해 1상에만 2년 가까이 걸렸다. 당초 관절염 환자를 겨냥했다가 통증 정도가 더 심한 암환자 등으로 대상을 확대하면서다. 투약한 약물의 반감기(약물이 체내에서 50%로 줄어드는 데 걸리는 시간)를 확인하는 게 현재 분석기술로 쉽지 않은 것도 임상이 더뎌진 이유다. OLP-1002 투약 용량은 다른 RNA 전문기업들이 개발 중인 신약 후보물질에 비해서도 1000분의 1에 불과하다. 정 대표는 “OLP-1002는 혈중 농도가 1ng에 그치기 때문에 분석이 쉽지 않았다”고 했다.
“내년 1분기 기술수출 기대”
올리패스의 핵심 기술은 PNA라 불리는 인공 유전자다. 세포투과성이 뛰어나 극미량으로도 효과를 볼 수 있다. 하지만 신기술인 만큼 동물실험은 물론 인체에서도 안전성과 효능을 입증하는 게 과제다. 정 대표는 “이번 임상에서 이런 부분을 상당히 해결했다”고 했다.올리패스는 OLP-1002에 거는 기대가 크다. 정 대표는 “기존 마약성 진통제는 내성 등의 부작용이 크지만 이를 해결할 비마약성 진통제는 아직 없다”며 “피하주사로 개발 중인 OLP-1002 개발이 성공하면 60조원의 세계 시장을 선점할 수 있을 것”이라고 했다.
OLP-1002의 효능이 조금씩 알려지면서 글로벌 제약사들이 관심을 보이고 있다. 정 대표는 “임상 1b상에서 OLP-1002의 효능이 확인되면 내년 1분기 중 기술수출이 가능할 것”이라고 했다.
파이프라인 임상 확대
올리패스는 당뇨성 망막증 치료제 ‘OLP-1003’의 전임상을 내년 시작할 예정이다. 임상1상 계획(IND)도 내년에 제출하는 게 목표다. 최근 유상증자에 성공하면서 자본잠식 우려를 씻었고 이 자금을 임상에 투입할 계획이다. 올리패스는 미국에서도 OLP-1003 임상에 나설 예정이다. 정 대표는 “2022년 미국 식품의약국(FDA)에 임상시험계획을 제출하고 2027년까지 시판 허가를 받는 게 목표”라고 했다.올리패스는 자회사 올리패스코스메슈티컬즈를 통해 진행하는 화장품 사업도 강화하기로 했다. 더마코스메틱(피부과학 화장품) 시장 강자로 꼽히는 닥터자르트가 롤모델이다. PNA의 세포투과력이 우수한 만큼 화장품 원료로도 승산이 있다고 보고 있다. 정 대표는 “아직 부족한 인지도에도 불구하고 콜라겐 크림 등은 시장에서 이미 수요가 꽤 있다”며 “지방을 태워 비만을 치료하는 후보물질의 원료로 화장품을 만들어 내년 출시할 예정”이라고 말했다.
이우상 기자 idol@hankyung.com

