식약처, 셀트리온 항체치료제 '렉키로나주' 허가 여부 5일 결정
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
마지막 자문 단계 '최종점검위원회' 개최
식품의약품안전처는 셀트리온의 신종 코로나바이러스 감염증(코로나19) 항체치료제 '렉키로나주'(성분명 레그단비맙·CT-P59)의 허가 여부를 오는 5일 결정한다고 1일 밝혔다.
식약처는 임상 2상 결과에 대한 마지막 전문가 자문 절차인 '최종점검위원회' 회의를 거쳐 허가를 최종적으로 정한다.
회의 결과는 당일 공개할 예정이다.
식약처는 코로나19 백신과 치료제의 정식 허가 전 검증자문단, 중앙약사심의위원회(중앙약심), 최종점검위원회로 이어지는 외부 전문가의 '삼중' 조언을 받고 있다.
이에 앞서 검증 자문단은 렉키로나주의 임상 3상 수행을 전제로 품목허가를 할 것을 권고했다.
렉키로나주는 임상 2상 결과 바이러스가 '음성'으로 전환되는 시간에서는 통계적 유의성을 나타내지 못했지만, 코로나19 증상 개선 시간은 3.43일 줄였다.
중앙약심도 '허가 가능' 결론을 내렸지만, 고위험군 경증 환자와 중등증 환자에 한정해서 투여해야 한다고 조건을 달았다.
경증 환자에게서는 통계적으로 유의한 수준의 치료 효과를 확인하지 못했다는 이유에서다.
식약처는 앞선 두 단계의 전문가 의견, 효능·효과, 권고사항 등을 종합해 최종점검위원회를 통해 렉키로나주의 허가 여부를 결정한다.
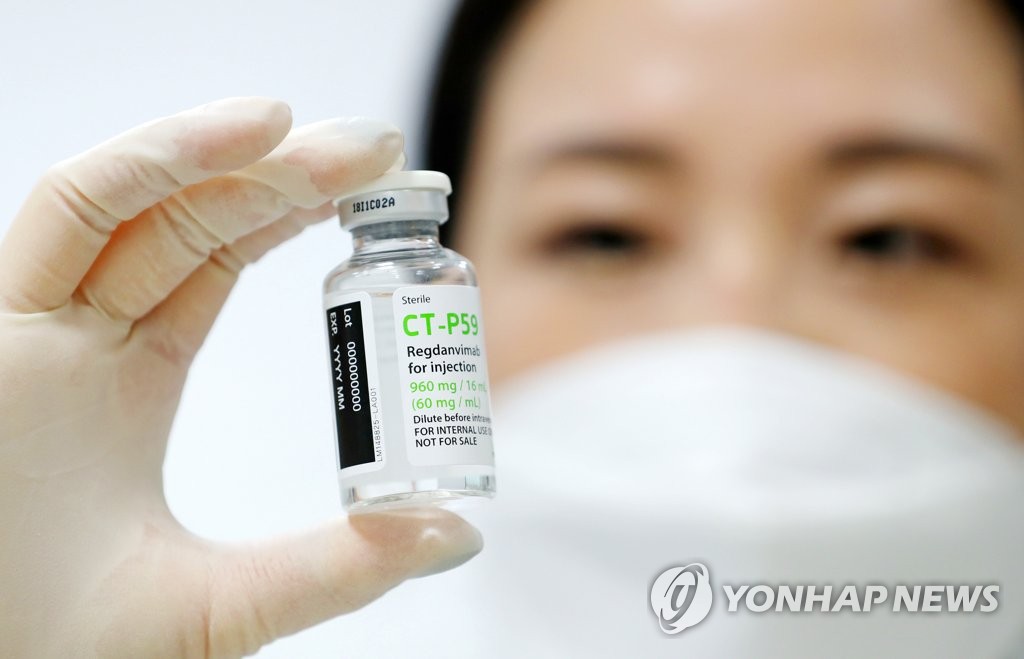
/연합뉴스
식품의약품안전처는 셀트리온의 신종 코로나바이러스 감염증(코로나19) 항체치료제 '렉키로나주'(성분명 레그단비맙·CT-P59)의 허가 여부를 오는 5일 결정한다고 1일 밝혔다.
식약처는 임상 2상 결과에 대한 마지막 전문가 자문 절차인 '최종점검위원회' 회의를 거쳐 허가를 최종적으로 정한다.
회의 결과는 당일 공개할 예정이다.
식약처는 코로나19 백신과 치료제의 정식 허가 전 검증자문단, 중앙약사심의위원회(중앙약심), 최종점검위원회로 이어지는 외부 전문가의 '삼중' 조언을 받고 있다.
이에 앞서 검증 자문단은 렉키로나주의 임상 3상 수행을 전제로 품목허가를 할 것을 권고했다.
렉키로나주는 임상 2상 결과 바이러스가 '음성'으로 전환되는 시간에서는 통계적 유의성을 나타내지 못했지만, 코로나19 증상 개선 시간은 3.43일 줄였다.
중앙약심도 '허가 가능' 결론을 내렸지만, 고위험군 경증 환자와 중등증 환자에 한정해서 투여해야 한다고 조건을 달았다.
경증 환자에게서는 통계적으로 유의한 수준의 치료 효과를 확인하지 못했다는 이유에서다.
식약처는 앞선 두 단계의 전문가 의견, 효능·효과, 권고사항 등을 종합해 최종점검위원회를 통해 렉키로나주의 허가 여부를 결정한다.

ADVERTISEMENT
ADVERTISEMENT





![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


