“아이큐어, 도네페질 패치 연내 승인 기대…본업가치 주목”
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
키움증권 분석
키움증권은 2일 아이큐어에 대해 연내 도네패질 치매 패치제의 국내 승인 및 생산이 시작된다며 본업의 진척에 관심을 가지라고 권고했다. 미국 임상 1상을 신청하며 해외 진출 지연에 대한 우려도 해소했다는 분석이다.
아이큐어의 전날 종가는 4만2350원이다. 회사의 주가는 모더나 백신 유통에 대한 기대감에 지난 2월15일 기준으로 7만8400원까지 급등했다. 하지만 기대감이 소멸되며 고점 대비 약 35%하락했다.
아이큐어는 셀트리온과 공동으로 도네페질 치매 패치제를 개발하고 있다. 지난 2월 임상 3상을 마치고 결과보고서를 검토 중이다. 회사는 한 달 내 최종보고서를 확정하고 상반기에 품목허가를 신청할 예정이다. 연내 승인을 받고 생산이 시작될 것이라는 예상이다.
허혜민 연구원은 “경구제 대비 패치제의 비열등성을 입증했기 때문에 허가가 반려될 가능성은 낮다”고 말했다.
국내 매출로 인한 실적 개선은 내년부터 발생할 것으로 봤다. 도네페질 패치는 임상 개시 단계에서 셀트리온과 공동판권 계약을 맺었다.
도네페질 치매 패치의 미국 진출도 첫 걸음을 내딛었다. 아이큐어는 지난달 30일에 미국 식품의약국(FDA)에 도네페질 패치에 대한 임상 1상을 신청했다. 건강한 성인 약 40명을 대상으로 경구제 아리셉트와 패치제의 효능을 비교하는 실험이다.
미국에서 임상을 수행하고 최종 품목허가를 받기까지는 3~4년이 소요될 것이란 전망이다. 당분간 추가 자금 조달에 대한 위험은 크지 않을 것으로 봤다. 지난 2월 이율 0%인 전환사채 500억원을 발행했기 때문이다.
허 연구원은 “미국에서 임상을 수행하고 최종 품목허가를 받기까지 3~4년이 소요될 것”“그동안 주가 상승의 발목을 잡았던 미국 진출 지연 리스크가 해소됐다는 데 의미가 있다”고 말했다.
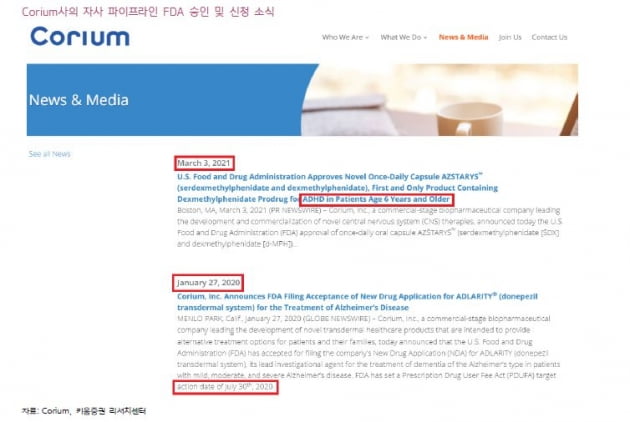
치매 도네페질 패치제에 대한 아이큐어의 유일한 경쟁사는 미국 코리움이다. 지난해 1월에 신약허가를 신청했지만, 아직 관련 소식을 전하지 않았다.
FDA 검토와 별개로 다른 후보물질에 집중하며 도네페질 패치제에 대한 우선순위가 낮아진 것이란 분석이다. 코리움은 지난달에 FDA로부터 6세 이상 환자의 주의력결핍과잉행동장애(ADHD) 치료제 승인 소식을 알렸다.
박인혁 기자 hyuk@hankyung.com
아이큐어의 전날 종가는 4만2350원이다. 회사의 주가는 모더나 백신 유통에 대한 기대감에 지난 2월15일 기준으로 7만8400원까지 급등했다. 하지만 기대감이 소멸되며 고점 대비 약 35%하락했다.
허혜민 연구원은 “경구제 대비 패치제의 비열등성을 입증했기 때문에 허가가 반려될 가능성은 낮다”고 말했다.
국내 매출로 인한 실적 개선은 내년부터 발생할 것으로 봤다. 도네페질 패치는 임상 개시 단계에서 셀트리온과 공동판권 계약을 맺었다.
미국에서 임상을 수행하고 최종 품목허가를 받기까지는 3~4년이 소요될 것이란 전망이다. 당분간 추가 자금 조달에 대한 위험은 크지 않을 것으로 봤다. 지난 2월 이율 0%인 전환사채 500억원을 발행했기 때문이다.
허 연구원은 “미국에서 임상을 수행하고 최종 품목허가를 받기까지 3~4년이 소요될 것”“그동안 주가 상승의 발목을 잡았던 미국 진출 지연 리스크가 해소됐다는 데 의미가 있다”고 말했다.

박인혁 기자 hyuk@hankyung.com
![[책마을] 뇌출혈 탓에 얄타회담 망친 루스벨트](https://img.hankyung.com/photo/202104/AA.25914836.3.jpg)



![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


