알츠하이머도 미토콘드리아 질환? 원인 단백질 연관성 발견
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
하버드 의대, 뉴런 내 아밀로이드 베타 생성 메커니즘 첫 규명
S1R 수용체, 치료 표적 부상…저널 '셀 리포츠' 논문
알츠하이머병의 원인 물질로 추정되는 아밀로이드 베타, 약칭 '아베타(Abeta)' 단백질이 어떤 과정을 거쳐 뇌 조직에 침적되는지를 미국 매사추세츠 제너럴 호스피털(MGH) 과학자들이 밝혀냈다.
아베타가 뇌 신경세포(뉴런)의 축삭돌기와 신경 말단에 쌓이면 뉴런 사이의 신호 전달이 제대로 이뤄지지 않아 인지 기능의 심한 장애를 일으킨다.
MGH 과학자들은 또 관련 분자 경로에서 아베타의 생성량 조절에 관여하는 특정 수용체도 찾아냈다.
알츠하이머병은 현재 근본적인 치료나 예방은 고사하고 진행 억제 치료도 하기 어려운 사실상의 불치병이다.
이번 연구는 아베타의 생성 메커니즘을 상세히 규명했다는 점에서 효과적인 치료법 개발에 근접했다는 평가가 나온다.
하버드 의대의 최대 수련병원인 MGH의 루돌프 탄지 박사 연구팀이 수행한 이 연구 결과는 18일(현지 시각) 저널 '셀 리포츠(Cell Reports)'에 논문으로 실렸다.
탄지 박사는 하버드 의대의 신경학과 석좌교수이며, 유전학과 알츠하이머병, 노화 등의 연구에서 세계적인 권위자로 알려져 있다.
탄지 박사팀은 1986년 알츠하이머병 관련 유전자를 처음 발견했다.
아베타 전구체(APP)의 생성 코드를 가진 것으로 유전자 이름도 똑같이 APP다.
전구체 APP가 베타·감마 두 종류의 세크레타아제(절단 효소)에 연속해 잘리면 부산물로 아밀로이드 베타가 생성된다.
기존의 알츠하이머병 연구는 이들 두 세크레타아제의 절단 작용을 막아 아베타의 생성을 차단하는 데 초점을 맞췄다.
하지만 이 접근법은 건강상의 안전 문제로 제동이 걸렸다.
연구팀은 2014년 개발한, '배양 접시의 알츠하이머병(Alzheimer's in a dish)'이라는 3차원 세포 모델을 이용해 아베타가 어떻게 생성되는지 파고들었다.
탄지 박사팀과 다른 MGH 과학자들은 2013년에 팔미토일화(palmitoylation)를 거친 APP 유형, 즉 palAPP가 아베타 생성에 관여한다는 것도 확인했다.
이는 뇌 신경세포의 palAPP가 '지질 뗏목(lipid raft·세포막 부유 지질 분자)'으로 알려진 소포에 실려 운반된다는 걸 시사한다.
그런데 여러 유형의 지질 뗏목 중에서 뇌의 신경망을 형성하는 신경 작용과 가장 많이 연관된 걸 다시 찾아야 했다.
팔미토일화란 지질 결합으로 단백질 활성이 변하는 걸 말한다.
이번에 연구팀은 '미토콘드리아 연관 내부원형질 망상 막(MAMs)'이라는 뉴런에서 조건에 맞는 지질 뗏목을 발견했다.
palAPP는 이런 지질 뗏목 안에서 베타 세크레타아제에 의해 절단될 수 있는 안정 상태를 유지했다.
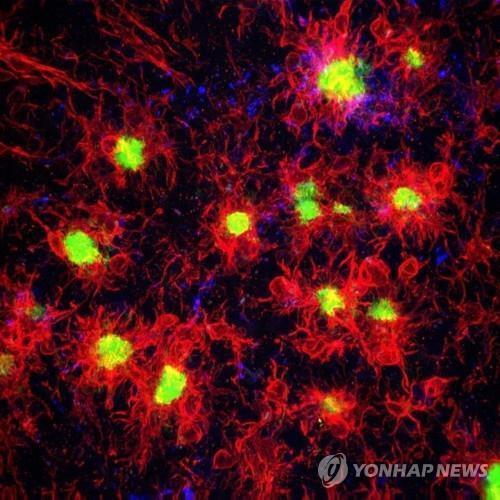
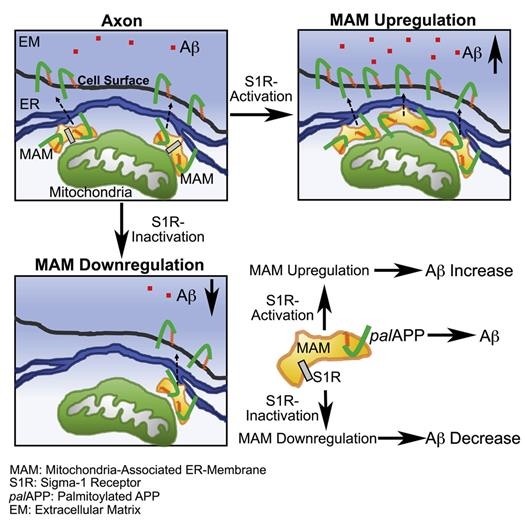
palAPP가 MAMs에서 베타 세크레타아제의 절단을 거치면 아밀로이드 베타 단백질이 생성된다는 게 입증되기는 처음이다.
알츠하이머병 환자의 뇌에서 MAMs가 증가하고 활성도가 높아지는 것으로 보고되긴 했지만, 아베타의 생성에 이렇게 직접 관여한다는 건 알지 못했다.
이번 연구에선 또 유전자 치료나 약물 투여로 '시그마-1 수용체(S1R)'의 발현을 막아 MAMs의 조립을 봉쇄하면, 베타 세크레타아제의 액손 내 palAPP 절단과 아베타 생성이 극적으로 감소한다는 것도 확인했다.
반대로 S1R을 활성화하면 베타 세크레타아제의 palAPP 절단과 액손 내 아베타 생성이 함께 증가했다.
탄지 교수는 "시그마-1 수용체가 특히 액손 내에서 아밀로이드 베타 생성을 억제하는, 중요한 약물 표적이 될 수 있다는 걸 시사한다"라고 말했다.
탄지 교수팀은 palAPP가 생성되는 APP 팔미토일화 과정을 바로 억제하는 치료 전략도 연구 중인데 이번 연구 결과가 큰 도움이 됐다고 한다.
연구팀은 아울러 MAMs에 직접 작용하는 ACAT라는 아베타 생성 억제제도 개발 중인 것으로 알려졌다.
혈액 검사 등을 통한 조기 검진에 맞춰 이런 치료제들을 적절히 투여하면 알츠하이머병의 진행을 멈추거나 속도를 늦추는 치료가 가능할 거로 연구팀은 기대한다.
/연합뉴스
S1R 수용체, 치료 표적 부상…저널 '셀 리포츠' 논문

알츠하이머병의 원인 물질로 추정되는 아밀로이드 베타, 약칭 '아베타(Abeta)' 단백질이 어떤 과정을 거쳐 뇌 조직에 침적되는지를 미국 매사추세츠 제너럴 호스피털(MGH) 과학자들이 밝혀냈다.
아베타가 뇌 신경세포(뉴런)의 축삭돌기와 신경 말단에 쌓이면 뉴런 사이의 신호 전달이 제대로 이뤄지지 않아 인지 기능의 심한 장애를 일으킨다.
MGH 과학자들은 또 관련 분자 경로에서 아베타의 생성량 조절에 관여하는 특정 수용체도 찾아냈다.
알츠하이머병은 현재 근본적인 치료나 예방은 고사하고 진행 억제 치료도 하기 어려운 사실상의 불치병이다.
이번 연구는 아베타의 생성 메커니즘을 상세히 규명했다는 점에서 효과적인 치료법 개발에 근접했다는 평가가 나온다.
하버드 의대의 최대 수련병원인 MGH의 루돌프 탄지 박사 연구팀이 수행한 이 연구 결과는 18일(현지 시각) 저널 '셀 리포츠(Cell Reports)'에 논문으로 실렸다.

탄지 박사는 하버드 의대의 신경학과 석좌교수이며, 유전학과 알츠하이머병, 노화 등의 연구에서 세계적인 권위자로 알려져 있다.
탄지 박사팀은 1986년 알츠하이머병 관련 유전자를 처음 발견했다.
아베타 전구체(APP)의 생성 코드를 가진 것으로 유전자 이름도 똑같이 APP다.
전구체 APP가 베타·감마 두 종류의 세크레타아제(절단 효소)에 연속해 잘리면 부산물로 아밀로이드 베타가 생성된다.
기존의 알츠하이머병 연구는 이들 두 세크레타아제의 절단 작용을 막아 아베타의 생성을 차단하는 데 초점을 맞췄다.
하지만 이 접근법은 건강상의 안전 문제로 제동이 걸렸다.
연구팀은 2014년 개발한, '배양 접시의 알츠하이머병(Alzheimer's in a dish)'이라는 3차원 세포 모델을 이용해 아베타가 어떻게 생성되는지 파고들었다.
탄지 박사팀과 다른 MGH 과학자들은 2013년에 팔미토일화(palmitoylation)를 거친 APP 유형, 즉 palAPP가 아베타 생성에 관여한다는 것도 확인했다.
이는 뇌 신경세포의 palAPP가 '지질 뗏목(lipid raft·세포막 부유 지질 분자)'으로 알려진 소포에 실려 운반된다는 걸 시사한다.
그런데 여러 유형의 지질 뗏목 중에서 뇌의 신경망을 형성하는 신경 작용과 가장 많이 연관된 걸 다시 찾아야 했다.
팔미토일화란 지질 결합으로 단백질 활성이 변하는 걸 말한다.
이번에 연구팀은 '미토콘드리아 연관 내부원형질 망상 막(MAMs)'이라는 뉴런에서 조건에 맞는 지질 뗏목을 발견했다.
palAPP는 이런 지질 뗏목 안에서 베타 세크레타아제에 의해 절단될 수 있는 안정 상태를 유지했다.

palAPP가 MAMs에서 베타 세크레타아제의 절단을 거치면 아밀로이드 베타 단백질이 생성된다는 게 입증되기는 처음이다.
알츠하이머병 환자의 뇌에서 MAMs가 증가하고 활성도가 높아지는 것으로 보고되긴 했지만, 아베타의 생성에 이렇게 직접 관여한다는 건 알지 못했다.
이번 연구에선 또 유전자 치료나 약물 투여로 '시그마-1 수용체(S1R)'의 발현을 막아 MAMs의 조립을 봉쇄하면, 베타 세크레타아제의 액손 내 palAPP 절단과 아베타 생성이 극적으로 감소한다는 것도 확인했다.
반대로 S1R을 활성화하면 베타 세크레타아제의 palAPP 절단과 액손 내 아베타 생성이 함께 증가했다.
탄지 교수는 "시그마-1 수용체가 특히 액손 내에서 아밀로이드 베타 생성을 억제하는, 중요한 약물 표적이 될 수 있다는 걸 시사한다"라고 말했다.
탄지 교수팀은 palAPP가 생성되는 APP 팔미토일화 과정을 바로 억제하는 치료 전략도 연구 중인데 이번 연구 결과가 큰 도움이 됐다고 한다.
연구팀은 아울러 MAMs에 직접 작용하는 ACAT라는 아베타 생성 억제제도 개발 중인 것으로 알려졌다.
혈액 검사 등을 통한 조기 검진에 맞춰 이런 치료제들을 적절히 투여하면 알츠하이머병의 진행을 멈추거나 속도를 늦추는 치료가 가능할 거로 연구팀은 기대한다.
/연합뉴스




![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


