약가 20억원, 희귀질환 유전자치료제 '졸겐스마'…국내 허가
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
보험급여 적용 여부 관심
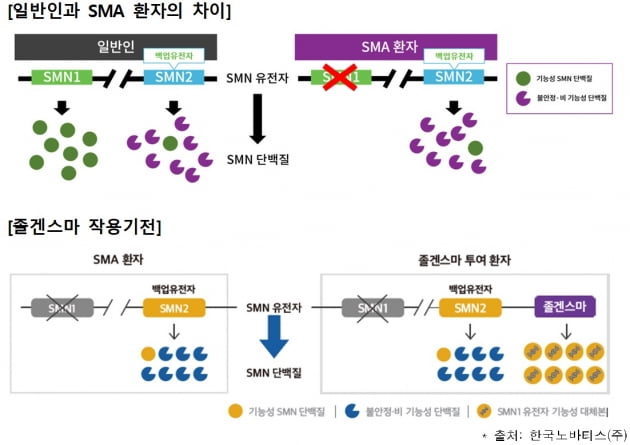
식품의약품안전처는 한국노바티스가 허가를 신청한 졸겐스마주를 두 번째 첨단바이오의약품으로 허가했다고 28일 밝혔다. 졸겐스마주는 '생존운동뉴런1'(SMN1) 유전자가 돌연변이 등으로 기능하지 못해 발생하는 퇴행성 신경질환 '척수성 근위축증'(SMA) 환자에게 정맥으로 일회 투여하는 치료제다.
척수성 근위축증은 세계적으로 신생아 1만명당 1명꼴로 발생하는 희귀질환이다. 졸겐스마주는 한 번만 맞으면 되기 때문에 환자들의 관심이 많다. 다만 초고가 의약품이기 때문에 보험급여 적용 여부가 관건이다.
졸겐스마주는 1회 투약비용이 미국에서 25억원, 일본에서는 약 18억9000만원으로 책정돼 있다. 졸겐스마주 급여 여부는 건강보험심사평가원 약제급여평가위원회에서 결정된다.
제약사가 약제급여 평가를 신청하면, 평가위가 120일 이내에 심의한다. 이후 국민건강보험공단과 제약사가 약가협상에 들어간다. 재평가 등의 절차가 추가로 발생하지 않는다면 보건복지부의 약가 고시까지 통상적으로 240일 이내 이뤄진다는 게 심평원의 설명이다.
졸겐스마주는 첨단재생바이오법에 따라 '장기추적조사' 대상 의약품으로 지정됐다. 제약사는 투여일로부터 15년 간 이상사례 등을 추적해야 한다. 또 처음 판매한 날부터 1년마다 장기추적조사한 내용과 결과 등을 식약처에 보고해야 한다.
한민수 기자


![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


