동화약품, 최대 7일 효과 장기 지속형 진통 주사제 국내 도입
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
대만 루모사와 계약
동화약품은 대만 루모사와 장기 지속형 진통 주사제 'LT1001'의 국내 도입 계약을 체결했다고 5일 밝혔다.
LT1001은 세계 최초로 최대 7일까지 효과가 지속되는 장기 지속형 진통제다. 근골격계 및 개복술, 제왕절개 등 다양한 수술을 시행하기 24시간 전 근육주사로 투여해 수술 후 통증 완화 목적으로 사용된다. 기존에 쓰이고 있는 통증 자가 조절법(PCA)에 비해 지속시간이 길다는 것이 장점이란 설명이다. 수술 직후 퇴원 또는 재활치료가 필요한 환자들의 편의성을 높일 것으로 기대된다.
LT1001은 높은 진통 효과를 가진 날부핀에 독자적인 제형 기술을 적용했다. 날부핀은 주사 후 혈중농도가 급격히 증가해 메스꺼움 구토 어지럼 등의 부작용 발생이 우려되는 것으로 알려져 있다. 날부핀의 안전성을 크게 개선한 LT1001은 긴 진통 효과로 마약성 경구 진통제 투여량을 감소시켜 주고, 잠재적인 약물 의존 가능성도 낮출 것으로 예상된다.
유준하 동화약품 대표는 "높은 성장세에 있는 국내 진통 주사제 시장에 환자들의 편의성 개선은 물론, 안전성까지 갖춘 혁신적인 신약을 선보이게 됐다"며 "루모사와의 협력에 이어 앞으로도 오픈 이노베이션 기회를 점차 넓혀갈 계획"이라고 말했다.
루모사는 대만의 신경성 및 염증성 질환 관련 혁신신약 개발업체다. LT1001의 한국 시장 인·허가 및 의약품 공급을 담당할 예정이다.
루모사의 룽진 린 최고경영자(CEO)는 "동화약품의 광범위한 마케팅망과 숙련된 영업 경험으로 LT1001이 한국 시장에서 높은 경쟁력을 가질 것으로 기대한다"고 했다.
동화약품은 이번 계약으로 LT1001의 국내 상업화 및 유통, 판매에 대해 독점적인 권한을 갖는다. 내년 2분기에 도입할 것으로 예상하고 있다. 지난해 국내 척추 임플란트 시장 1위 기업인 메디쎄이를 인수한 동화약품은 LT1001 도입으로 외과수술 시장 공략을 본격적으로 진행할 계획이다.
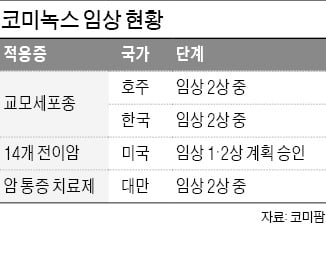
LT1001은 현재 대만 및 싱가포르서 승인을 획득했다. 태국과 말레이시아에서는 허가 절차를 밟는 중이다. 또 시판 허가를 위해 중국과 미국에서 각각 임상 3상과 1상이 진행되고 있다.
한민수 기자
LT1001은 세계 최초로 최대 7일까지 효과가 지속되는 장기 지속형 진통제다. 근골격계 및 개복술, 제왕절개 등 다양한 수술을 시행하기 24시간 전 근육주사로 투여해 수술 후 통증 완화 목적으로 사용된다. 기존에 쓰이고 있는 통증 자가 조절법(PCA)에 비해 지속시간이 길다는 것이 장점이란 설명이다. 수술 직후 퇴원 또는 재활치료가 필요한 환자들의 편의성을 높일 것으로 기대된다.
LT1001은 높은 진통 효과를 가진 날부핀에 독자적인 제형 기술을 적용했다. 날부핀은 주사 후 혈중농도가 급격히 증가해 메스꺼움 구토 어지럼 등의 부작용 발생이 우려되는 것으로 알려져 있다. 날부핀의 안전성을 크게 개선한 LT1001은 긴 진통 효과로 마약성 경구 진통제 투여량을 감소시켜 주고, 잠재적인 약물 의존 가능성도 낮출 것으로 예상된다.
유준하 동화약품 대표는 "높은 성장세에 있는 국내 진통 주사제 시장에 환자들의 편의성 개선은 물론, 안전성까지 갖춘 혁신적인 신약을 선보이게 됐다"며 "루모사와의 협력에 이어 앞으로도 오픈 이노베이션 기회를 점차 넓혀갈 계획"이라고 말했다.
루모사는 대만의 신경성 및 염증성 질환 관련 혁신신약 개발업체다. LT1001의 한국 시장 인·허가 및 의약품 공급을 담당할 예정이다.
루모사의 룽진 린 최고경영자(CEO)는 "동화약품의 광범위한 마케팅망과 숙련된 영업 경험으로 LT1001이 한국 시장에서 높은 경쟁력을 가질 것으로 기대한다"고 했다.
동화약품은 이번 계약으로 LT1001의 국내 상업화 및 유통, 판매에 대해 독점적인 권한을 갖는다. 내년 2분기에 도입할 것으로 예상하고 있다. 지난해 국내 척추 임플란트 시장 1위 기업인 메디쎄이를 인수한 동화약품은 LT1001 도입으로 외과수술 시장 공략을 본격적으로 진행할 계획이다.
LT1001은 현재 대만 및 싱가포르서 승인을 획득했다. 태국과 말레이시아에서는 허가 절차를 밟는 중이다. 또 시판 허가를 위해 중국과 미국에서 각각 임상 3상과 1상이 진행되고 있다.
한민수 기자