“GC녹십자, 백신 판매 및 유통으로 하반기 실적 성장 전망”
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
대신증권 분석
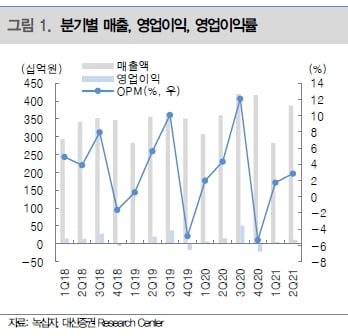
GC녹십자의 올 2분기 매출과 영업이익은 각각 3867억원과 111억원을 기록했다. 전년 동기 대비 매출은 7.7% 늘고 영업이익은 28.7% 줄었다. 영업이익은 판매관리비가 증가하며 시장 전망치를 59% 밑돌았다.
회사에 따르면 2분기 남반구에 독감 백신을 유리병(바이알) 제형이 아닌 사전충전형 주사(프리필드 시린지) 형태로 수출하며 운임비가 증가했다. 일반의약품(OTC) 관련 광고선전비도 늘었다. 다만 하반기에는 북반구에 유리용기(바이알) 형태로 수출할 예정이라 운임비 증가는 일회성 요인일 가능성이 높다는 설명이다. 하반기에는 새로운 의약품 광고도 없을 계획이다.
하반기 독감 백신 매출은 내수 1200억원과 수출 260억원으로 예상했다. 하반기 모더나 코로나19 백신 유통 관련 정부와의 계약 규모는 350억원이다.
녹십자는 다수의 코로나19 백신 개발사와 위탁생산(CMO)에 대해 지속적으로 논의하고 있다고 했다. 그러나 현재 주요 개발사들이 개별 국가를 중심으로 우선 공급하고 있어, CEPI를 통한 공급은 후순위인 상황이다. 이에 따라 계약 시점을 예측하기는 어렵다고 봤다. CEPI는 올해 코로나19 백신 생산 및 공급 물량으로 20억도즈를 제시했지만 이행율은 5% 미만이다.
임윤진 연구원은 “공급은 여전히 부족한 상황이라 본계약 체결 가능성이 있다”며 “내년 5월까지 계약 기간을 연장할 수 있어 우려할 부분은 아니다”고 판단했다.
신약 개발도 차질 없이 진행 중이다. 혈액제제인 ‘IVIG SN 10%’는 미국 허가 절차를 밟고 있다. 오는 9~10월 미국 식품의약국(FDA)의 공장 실사가 예상된다. 내년 2월25일까지 허가 여부가 결정될 예정이다. 지연 없이 허가를 획득하면, 내년 하반기 출시할 계획이다.
혈우병 치료제인 ‘그린진에프’는 3분기 내에 중국에서 승인을 받아 내년 상반기에 출시할 예정이다. 헌터증후군 치료제인 ‘헌터라제’는 작년 9월에 중국 허가를 받고 각 성별로 약가를 협상하고 있다. 연내 7~8개 성에서 협상을 완료하고 내년 상반기에 출시하겠다는 목표다.
박인혁 기자



![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


