헬릭스미스 "2023년부터 신약 동시다발 임상"
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
기자간담회서 사업계획 공개
엔젠시스, 2년내 품목허가 계획
다른 치료제도 임상 진입 예정
"유전자세포치료제 위탁생산시설
이달 준공…年 매출 100억 목표"
엔젠시스, 2년내 품목허가 계획
다른 치료제도 임상 진입 예정
"유전자세포치료제 위탁생산시설
이달 준공…年 매출 100억 목표"

헬릭스미스 경영진이 엔젠시스 의존도를 낮추는 데 힘을 쏟기로 한 이유다. 유승신 헬릭스미스 대표는 15일 온라인 기자간담회를 열고 엔젠시스를 제외한 8개 신약 후보물질을 이른 시일 내에 임상 1상 단계에 올려놓겠다고 밝혔다. 또 유전자 치료제 위탁개발생산(CDMO) 사업을 ‘캐시카우(현금창출원)’로 키운다는 청사진도 내놨다.
“8개 파이프라인 본격 임상 가동”
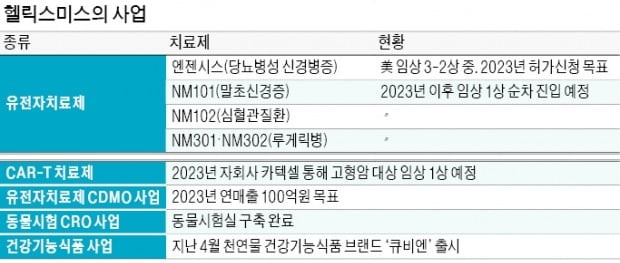
CAR-T 치료제는 2023년 자회사 카텍셀을 통해 신경모세포종 등 고형암을 대상으로 한 임상 1상을 추진하기로 했다. 헬릭스미스는 △엔젠시스를 제외한 DNA 기반 후보물질 2개 △아데노바이러스 기반 후보물질 2개 △CAR-T 후보물질 4개를 보유하고 있다.
헬릭스미스가 임상 대상을 늘리는 건 엔젠시스 의존도를 떨어뜨리기 위해서다. 사업 포트폴리오를 확대해야 위험을 분산할 수 있다는 판단에서다.
여윳돈이 있다는 점도 공격적인 임상계획에 영향을 미쳤다. 서제희 헬릭스미스 전략기획본부장은 “2000억원이 넘는 현금 및 현금성 자산을 확보하는 등 충분한 유동성을 갖췄다”며 “내년에 계획한 임상을 예정대로 끝내도 1000억원이 넘는 현금성 자산이 남을 것”이라고 말했다.
엔젠시스에 대해선 2023년까지 임상 3상을 끝내고 미국 품목허가를 신청하기로 했다. 이 회사는 엔젠시스의 두 번째 임상 3상을 미국에서 진행하고 있다.
유전자 치료제 CDMO 진출
신사업으로 추진하고 있는 유전자 치료제 CDMO 사업도 조만간 궤도에 오를 전망이다. 이 회사는 지난 13일 서울 마곡동에 있는 유전자치료제 생산시설 준공식을 열었다. 유전자 치료제 CDMO 사업에서 내년 2~3월에 첫 매출을 낸 뒤 이르면 2023년 연매출 100억원을 내는 게 목표다. 국내 40여 개 바이오 기업이 잠재 고객이다.유전자 치료제 CDMO 사업은 삼성바이오로직스 등 다른 바이오 기업들도 추진 중이다. 유전자 치료제를 직접 개발했던 경험을 적극 살리면 차별화가 가능하다는 게 헬릭스미스 측의 판단이다. 서 본부장은 “20년 이상 유전자 치료제를 개발하면서 개발사 입장에서 신약 개발의 어려움이 어디서 생기는지를 알고 있다는 게 강점”이라며 “자회사의 CAR-T 치료제 임상 제품을 공급할 때도 이 생산시설을 활용할 수 있다”고 설명했다.
자체 전임상에 사용했던 동물시험 시설도 임상수탁기관(CRO) 사업에 활용해 수익원을 다각화하기로 했다. 이 회사는 지난 4월 천연물 기반 건강기능식품 브랜드인 ‘큐비엔’도 출시했다. 그간 내수용 원료 공급 위주로 진행했던 건강기능식품 사업을 완제품 공급 중심으로 전환하기 위한 취지다.
이주현 기자 deep@hankyung.com


![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


