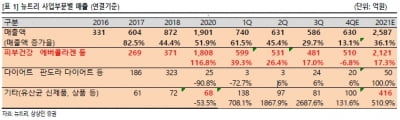
박재경 연구원은 22일 “제약·바이오 업종의 원 성장동력인 R&D에 주목하라”고 했다. 국내 제약바이오 기업이 세계 시장에서 꾸준히 주목받고 있으며, 일부 신약은 미국 식품의약국(FDA) 승인을 앞두고 있다는 것이다.
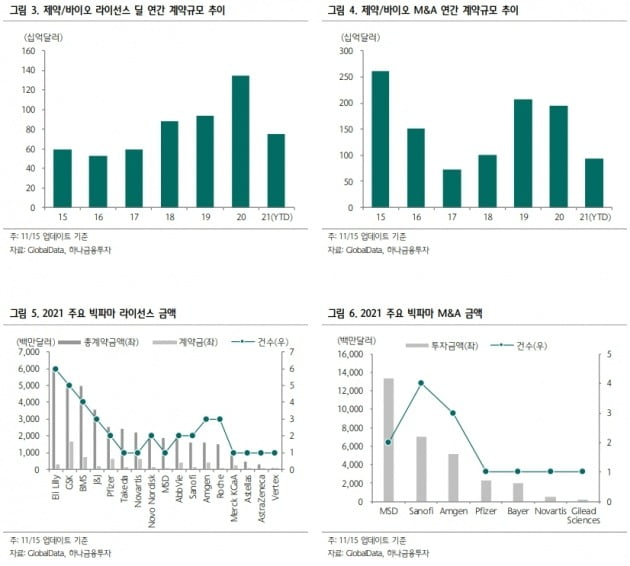
지씨셀은 제대혈 유래 자연살해(NK) 세포치료제의 최초 임상 결과 발표를 앞두고 있다. 레고켐바이오도 자체 항체약물접합체(ADC) 플랫폼의 최초 임상 결과가 내년 상반기에 나올 것으로 봤다.
바이오시밀러(바이오의약품 복제약) 시장에 대한 전망도 내놨다. 블록버스터(연 매출 10억달러 이상 의약품)의 특허 만료가 대거 예정돼있는 점이 성장동력이 될 것이란 분석이다.
향후 10년간 ‘루센티스’ ‘아일리아’ 등 안과 질환 블록버스터와 ‘키트루다’ ‘옵디보’를 필두로 한 면역항암제 블록버스터들의 특허 만료가 기다리고 있다. 특허 만료 의약품의 개수 역시 과거 10년에 비해 2배에 달할 것으로 전망했다.
내년 승인단계에 진입하는 국산 신약에도 관심을 가질 것을 권고했다. 녹십자의 면역결핍치료제 ‘IVIG-SN 10%’와 메지온의 ‘쥴비고’(성분명 유데나필)는 1분기 내에 FDA 승인 여부가 결정될 것으로 봤다. 제조시설 결함으로 지난 8월 최종보완요구서(CRL)를 수령한 한미약품의 ‘롤론티스’는 품목허가(BLA) 재신청이 상반기 내 이뤄진다면 내년 중 FDA 승인이 가능할 것이란 전망이다.
유한양행·오스코텍의 ‘렉라자’(성분명 레이저티닙)는 올해 유럽종양학회(ESMO)에서 발표한 임상 결과를 근거로 가속 승인을 신청한다면, 내년 허가 및 출시가 가능할 것으로 예상했다. 레이저티닙은 2019년 얀센에 기술이전됐다.
최선호주로는 삼성바이오로직스와 유한양행을 제시했다. 삼성바이오로직스에 대해서는 내년에도 위탁생산(CMO) 수요는 꾸준할 것이라며 빠른 증설을 통해 이에 대응할 수 있을 것이라 분석했다.
박 연구원은 “삼성바이오로직스는 4공장 증설에 이어 제2바이오캠퍼스에 들어설 5~6공장 증설도 계획 중”이라며 “5~6공장에는 기존의 동물세포 CMO 설비 외에 추가로 유전자·세포 치료제(GCT) 설비가 포함될 예정으로 이를 통해 기업의 장기적인 성장 그림이 확인돼 이에 따른 재평가(리레이팅)가 전망된다”고 했다.
유한양행에 대해서는 내년부터 R&D 투자의 결실을 맺을 것이라 봤다. 레이저티닙이 타그리소 내성 환자 대상 우수한 반응률을 보인 만큼 내년 가속 승인을 통한 글로벌 시장 진출을 기대했다.
이도희 기자