백신 운반체 바이러스는 어떻게 외부 DNA를 세포핵에 전달할까
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
고도로 진화한 DNA 전달 메커니즘 처음 밝혀져
바이러스 단백질 V, 세포 효소 Mib 1 핵심 역할
스위스 취리히대 연구진, 저널 '사이언스 어드밴시스'에 논문

지금까지 척추동물에서 발견된 아데노바이러스(Adenovirus)는 약 50종에 달한다.
그중 인간 아데노바이러스는 주로 소아에게 호흡기 질환을 일으킨다.
아데노바이러스는 오래전부터 백신의 운반체(vector)로 쓰였다.
세포 배양이 쉽고 유전자 조작이 간편하기 때문이다.
코로나19(신종 코로나바이러스 감염증) 백신중에도 그런 경우가 있다.
아스트라제네카, 존슨앤드존슨, 스푸트니크 V 등은 복제 능력을 제거한 아데노바이러스를 운반체로 이용해 제조된 것이다.
이런 백신을 맞으면 신종 코로나바이러스의 스파이크 단백질이 세포 표면에 제시돼 면역 반응을 일으킨다.
그렇다면 아데노바이러스는 어떻게 외부 DNA, 즉 스파이크 단백질의 생성 코드가 담긴 DNA를 세포핵 안으로 운반하는 걸까.
매우 정교하게 진화된 아데노바이러스의 DNA 전달 메커니즘을 스위스 취리히대 과학자들이 처음 밝혀냈다.
여기서 핵심 역할을 하는 건 아데노바이러스의 '단백질 V'와 숙주 세포의 '마인드 봄 1(Mib 1) 효소였다.
바이러스 단백질 V는 바이러스 DNA가 단백질 외피와 단단히 결합하게 하는 기능을 했다.
Mib 1 효소는 바이러스 입자가 세포핵 안으로 DNA를 방출할 때 단백질 외피를 벗겨내는 데 필요했다.
취리히대(UZH) 분자 생명과학과의 우르스 그레버 교수팀이 수행한 이 연구 결과는 지난 17일(현지 시각) 저널 '사이언스 어드밴시스(Science Advances)'에 논문으로 실렸다.
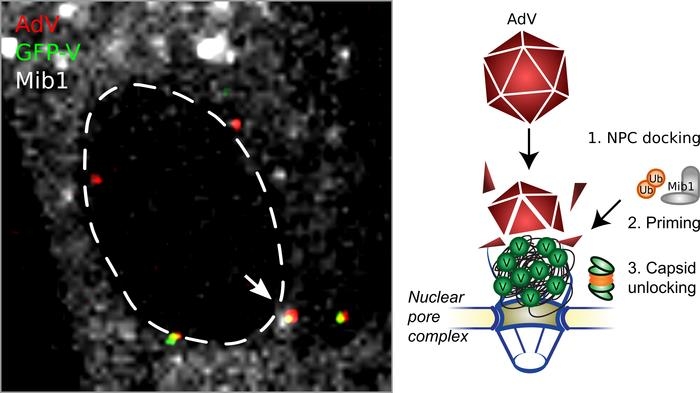
바이러스의 DNA를 둘러싼 단백질 외피는, 숙주 세포가 외부에서 들어온 DNA를 감지해 비상경보를 작동하는 걸 막는다.
바이러스 입자는 세포핵의 출입문 격인 '핵 기공 복합체(nuclear pore complex)'에 도달하면 세포핵 안으로 DNA를 방출한다.
그러면 숙주세포의 복제 기계가 바이러스의 유전 정보를 읽고 거기에 해당하는 단백질을 만들어낸다.
인체 세포에 감염한 바이러스의 증식은 이렇게 이뤄진다.
그런데 단백질 V가 없으면 이 메커니즘이 제대로 작동하지 못하는 것으로 밝혀졌다.
이 단백질이 결핍된 아데노바이러스는 구조적 안정성이 떨어져, 핵 기공 복합체에 도달하기 훨씬 전에 DNA를 쏟아냈다.
이렇게 너무 빨리 DNA를 내보내면 바이러스의 감염력이 약해지고, 면역계를 자극하는 반응도 촉발했다.
이런 면역계 자극 반응이 너무 강하면 염증으로 이어졌다.
코로나19 백신이 강한 면역 반응을 유도하려면 이 면역계 자극 반응이 아주 적정한 수준으로 일어나야 했다.
그건 아데노바이러스와 같은 운반체 기반 백신이든, 전혀 다른 방식의 mRNA 백신이든 차이가 없었다.
운반체 기반 백신의 바이러스 입자가 핵 기공 복합체까지 이동해 DNA를 방출하는 과정에서 DNA를 감싼 단백질 외피가 매우 중요한 역할을 했다.
특히 운반체 기반 백신이 효능을 발휘하려면 이 외피의 탈각(uncoating)이 절대적으로 필요했다.
바이러스 입자가 너무 크면 핵 기공 복합체를 통해 세포핵으로 진입할 수 없기 때문이다.
단백질 외피가 적당한 시점에 벗겨지는 덴 Mib 1 효소가 결정적인 작용을 했다.
이 효소가 활성화하면 단백질 V의 성질이 변해 DNA를 감쌌던 단백질 외피가 분해됐다.
그레버 교수는 "이번 연구 결과가, 병든 세포에 유전자를 전달하는 치료 절차의 개선과 항바이러스 치료법의 개발을 자극할 것"이라고 말했다.
특히 아데노바이러스는 다양한 방법으로 활용될 가능성이 크다고 한다.
예를 들면 환자의 유전자를 편집해 유전 질환, 대사 질환, 암 등을 치료하려고 할 때 DNA 운반체로 쓰기에 제격이라고 과학자들은 말한다.
/연합뉴스
바이러스 단백질 V, 세포 효소 Mib 1 핵심 역할
스위스 취리히대 연구진, 저널 '사이언스 어드밴시스'에 논문

지금까지 척추동물에서 발견된 아데노바이러스(Adenovirus)는 약 50종에 달한다.
그중 인간 아데노바이러스는 주로 소아에게 호흡기 질환을 일으킨다.
아데노바이러스는 오래전부터 백신의 운반체(vector)로 쓰였다.
세포 배양이 쉽고 유전자 조작이 간편하기 때문이다.
코로나19(신종 코로나바이러스 감염증) 백신중에도 그런 경우가 있다.
아스트라제네카, 존슨앤드존슨, 스푸트니크 V 등은 복제 능력을 제거한 아데노바이러스를 운반체로 이용해 제조된 것이다.
이런 백신을 맞으면 신종 코로나바이러스의 스파이크 단백질이 세포 표면에 제시돼 면역 반응을 일으킨다.
그렇다면 아데노바이러스는 어떻게 외부 DNA, 즉 스파이크 단백질의 생성 코드가 담긴 DNA를 세포핵 안으로 운반하는 걸까.
매우 정교하게 진화된 아데노바이러스의 DNA 전달 메커니즘을 스위스 취리히대 과학자들이 처음 밝혀냈다.
여기서 핵심 역할을 하는 건 아데노바이러스의 '단백질 V'와 숙주 세포의 '마인드 봄 1(Mib 1) 효소였다.
바이러스 단백질 V는 바이러스 DNA가 단백질 외피와 단단히 결합하게 하는 기능을 했다.
Mib 1 효소는 바이러스 입자가 세포핵 안으로 DNA를 방출할 때 단백질 외피를 벗겨내는 데 필요했다.
취리히대(UZH) 분자 생명과학과의 우르스 그레버 교수팀이 수행한 이 연구 결과는 지난 17일(현지 시각) 저널 '사이언스 어드밴시스(Science Advances)'에 논문으로 실렸다.

바이러스의 DNA를 둘러싼 단백질 외피는, 숙주 세포가 외부에서 들어온 DNA를 감지해 비상경보를 작동하는 걸 막는다.
바이러스 입자는 세포핵의 출입문 격인 '핵 기공 복합체(nuclear pore complex)'에 도달하면 세포핵 안으로 DNA를 방출한다.
그러면 숙주세포의 복제 기계가 바이러스의 유전 정보를 읽고 거기에 해당하는 단백질을 만들어낸다.
인체 세포에 감염한 바이러스의 증식은 이렇게 이뤄진다.
그런데 단백질 V가 없으면 이 메커니즘이 제대로 작동하지 못하는 것으로 밝혀졌다.
이 단백질이 결핍된 아데노바이러스는 구조적 안정성이 떨어져, 핵 기공 복합체에 도달하기 훨씬 전에 DNA를 쏟아냈다.
이렇게 너무 빨리 DNA를 내보내면 바이러스의 감염력이 약해지고, 면역계를 자극하는 반응도 촉발했다.
이런 면역계 자극 반응이 너무 강하면 염증으로 이어졌다.
코로나19 백신이 강한 면역 반응을 유도하려면 이 면역계 자극 반응이 아주 적정한 수준으로 일어나야 했다.
그건 아데노바이러스와 같은 운반체 기반 백신이든, 전혀 다른 방식의 mRNA 백신이든 차이가 없었다.
운반체 기반 백신의 바이러스 입자가 핵 기공 복합체까지 이동해 DNA를 방출하는 과정에서 DNA를 감싼 단백질 외피가 매우 중요한 역할을 했다.
특히 운반체 기반 백신이 효능을 발휘하려면 이 외피의 탈각(uncoating)이 절대적으로 필요했다.
바이러스 입자가 너무 크면 핵 기공 복합체를 통해 세포핵으로 진입할 수 없기 때문이다.
단백질 외피가 적당한 시점에 벗겨지는 덴 Mib 1 효소가 결정적인 작용을 했다.
이 효소가 활성화하면 단백질 V의 성질이 변해 DNA를 감쌌던 단백질 외피가 분해됐다.

그레버 교수는 "이번 연구 결과가, 병든 세포에 유전자를 전달하는 치료 절차의 개선과 항바이러스 치료법의 개발을 자극할 것"이라고 말했다.
특히 아데노바이러스는 다양한 방법으로 활용될 가능성이 크다고 한다.
예를 들면 환자의 유전자를 편집해 유전 질환, 대사 질환, 암 등을 치료하려고 할 때 DNA 운반체로 쓰기에 제격이라고 과학자들은 말한다.
/연합뉴스
ADVERTISEMENT
ADVERTISEMENT


![[속보] 경찰 수사심의위 "장경태 준강제추행 혐의 송치해야"](https://img.hankyung.com/photo/202603/01.42941005.3.jpg)

![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


