영상 카드와 함께 카톡 선물 보내세요~
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
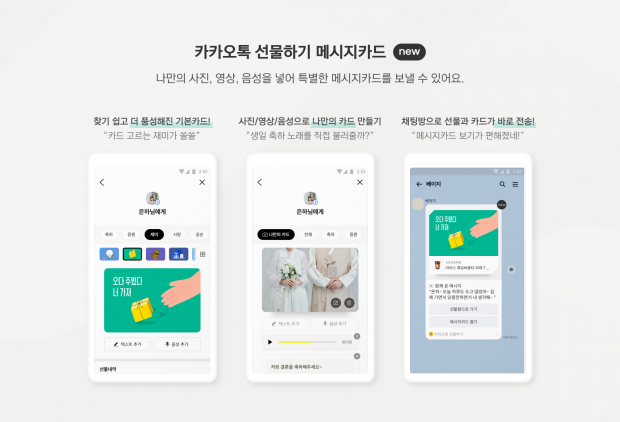
︎ 대면으로 느낄 수 있는 정성과 고마움∙축하 등의 감정까지 전달해 ‘비대면 선물 경험’ 강화
(2021/1/4) 카카오톡 선물하기가 선물과 함께 발송할 수 있는 메시지카드 기능을 대폭 개편한다.
가장 큰 변화는 장문의 메시지 및 사진/영상/음성을 활용한 나만의 메시지카드 작성이 가능한 것이다. 작성 가능한 글자수가 60자에서 100자로 늘어나며, 기본으로 제공하는 카드 디자인 외에 이용자가 휴대폰/PC에서 사진이나 영상을 불러와 나만의 메시지카드를 만들고 음성 메시지도 녹음해 보낼 수 있다.
예를 들어, 생일을 맞은 친구에게 생일 축하 메시지를 녹음하거나 안부 인사를 담은 영상을 촬영해 메시지카드 형식으로 선물과 함께 전달하는 것이 가능하다.
또한, 기본 제공하는 메시지카드의 경우 기존 9개의 디자인에서 축하/감사/재미/공손 등 선물 목적에 따라 6개의 테마로 분류해 50여 종으로 가짓수를 확대해 제공한다.
이 외에도 선물하기에 입점한 일부 브랜드의 경우 브랜드 로고 등이 적용된 전용 메시지카드도 제공하며, 설날/크리스마스 등 시즌을 테마로 한 메시지카드도 선보일 예정이다.
더불어, 선물하기는 선물을 받는 사람이 대화창에서 메시지카드를 놓치지 않고 쉽게 확인할 수 있도록 사용성도 높였다.
선물 수신 메시지 전면에 메시지카드를 노출하고, 선물을 수신할 때 애니메이션 효과와 함께 메시지카드를 확인할 수 있게 하는 등 메시지카드 수신 경험도 이전보다 직관적으로 개선했다.
또한, 메시지카드 저장 기능도 추가돼 간직하고 싶은 메시지카드를 따로 보관할 수 있고 SNS에 공유도 가능하며, 개편된 ‘주고받은 선물추억’ 페이지를 통해 시간이 지나도 이용자간 선물 이력과 메시지카드를 한 데 모아 편리하게 확인 할 수 있다.
카카오톡 선물하기는 이번 개편을 통해 선물하기에서만 제공할 수 있는 선물 경험을 강화한다는 계획이다. 카카오톡이라는 강력한 플랫폼 안에서 대면으로만 느낄 수 있었던 고마움∙축하 등의 감정까지 비대면 선물을 통해서 전달할 수 있도록 해, 관계지향적인 커머스 경험을 완성해 나갈 예정이다.
카카오톡 선물하기 관계자는 “비대면 선물 시장이 성장하면서 선물하기 내 상품군 확대와 더불어 고마운 마음을 전달하는 것에도 소홀함이 없도록 메시지카드 기능을 개편했다” 며 “나만의 메시지카드를 통해 비대면으로 주는 선물이 더욱 특별하게 다가오는 경험을 이용자들에게 제공하겠다” 고 말했다.
ADVERTISEMENT
ADVERTISEMENT




![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


