수노시는 SK바이오팜이 개발한 수면장애 치료제다. 기면증 또는 폐쇄성 수면 무호흡증(OSA)으로 인한 과도한 졸림(EDS)에 처방된다. EDS를 막기 위해 방출되는 ‘도파민’과 ‘노르에피네프린’이 세포 내로 재흡수되는 것을 억제하는 기전을 가지고 있다. 이들이 세포 밖에 있어야 EDS를 막는 역할을 하기 때문이다.
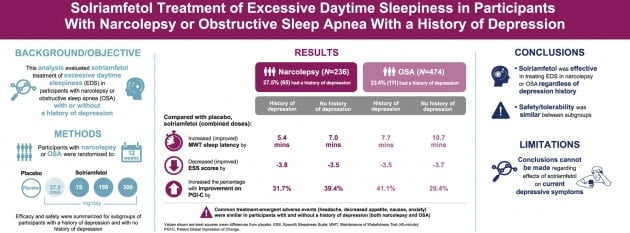
기면증 또는 OSA 환자들은 높은 비율로 우울증을 경험한다. 이번 사후 분석을 진행한 배경이다. 분석 결과 약의 안전성 및 효능은 환자의 우울증 병력에 영향을 받지 않았다. 수노시는 우울증 임상 병력이 있는 환자와 없는 환자 모두의 EDS 증상을 위약 대비 개선했다.
분석은 기면증 또는 OSA 관련 EDS가 있는 성인 환자를 대상으로 이뤄졌다. 전체 참가자 중 기면증 환자의 27.5%(236명 중 65명)와 OSA 환자의 23.4%(474명 중 111명)가 우울증 병력이 있었다.
이들은 12주간 위약 또는 수노시를 처방받았다. 수노시의 경우 1일 37.5mg(OSA만 해당), 75mg, 150mg 또는 300mg 투약군에 무작위 배정됐다.
분석 결과 기면증 환자 중 우울증이 있는 경우와 그렇지 않은 경우 모두 평가 점수가 위약 대비 개선됐다. 40분간 각성유지검사(MWT40) 평균 점수는 우울증이 있는 참가자는 위약 대비 5.4분, 없는 환자는 7분 증가했다. 앱워스(Epworth) 졸음 척도(ESS) 점수는 3.8점과 3.5점 줄었다. 환자의 전체적인 인상 변화(PGI-C) 점수가 개선된 환자의 비율은 우울증이 있는 경우 31.7%, 없는 경우 39.4% 위약 대비 높았다.
OSA에서도 비슷한 결과가 도출됐다. MWT40의 경우 우울증 병력이 있는 참가자는 7.7분, 없는 참가자는 10.7분이 위약 대비 늘었다. ESS는 3.5점 및 3.7점 감소했다. PGI-C가 개선된 참가자 비율은 각각 41.1% 및 29.4% 위약 대비 많았다.
일반적인 치료 관련 부작용(두통, 식욕 감소, 메스꺼움, 불안)도 우울증 병력이 있는 참가자 및 없는 참가자 간 유사했다. 다만 수노시가 우울증을 극복하는 의미는 아니라고 액섬은 설명했다.
액섬은 아시아 12개국을 제외한 수노시의 세계 판권을 보유하고 있다. 수노시는 2019년 미국 식품의약국(FDA), 2020년 유럽 의약품청(EMA)에서 품목허가를 받았다. 지난해부터는 캐나다에서도 시판이 가능해졌다.
액섬은 수노시에 대해 기존 EDS 외에 주의력결핍 과다행동장애(ADHD) 치료 임상에 새롭게 착수할 계획이다. 올 4분기 임상 2·3상을 시작해 내년 하반기 주요결과(톱라인)를 확보할 수 있을 것이란 예상이다.
수노시의 미국 EDS 치료제 잠재 매출을 연간 약 3억~5억달러로 보고 있다. 여기에 신규 적응증을 포함하면 연 10억달러까지 가능할 것으로 추산했다.
이도희 기자 tuxi0123@hankyung.com


![FDA 자문위, 아밀릭스 새 루게릭병 치료제 승인 권고 [이우상의 글로벌워치]](https://img.hankyung.com/photo/202209/01.31165598.3.jpg)




