갑상선안병증藥 선두주자 호라이즌, 피하주사 개발 시작
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
테페자, 2020년 정맥주사로 美 허가
한올바이오파마, 연내 TED 美 3상
한올바이오파마, 연내 TED 美 3상
제리스바이오파마는 지난 23일(현지시간) 호라이즌테라퓨틱스와 이 회사의 테페자를 SC제형으로 개발하는 연구협력(리서치 콜라보레이션) 계약을 체결했다고 밝혔다.
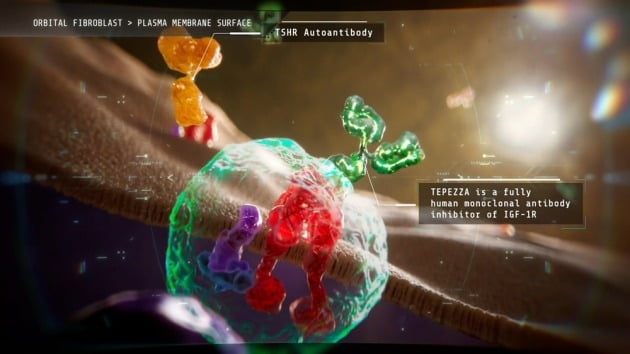
갑상선안병증은 자가면역질환의 일종이다. 자가항체가 '인슐린유사성장인자1 수용체(IGF1R)'와 결합해 안와(머리뼈 속 안구가 들어있는 공간) 섬유아세포를 자극하며 발병한다. 활성화된 섬유아세포가 눈 주위의 근육과 지방조직을 공격해 안구돌출 등을 유발한다. 사물이 두 개로 보이거나 각막에 궤양이 생기기도 한다. 그동안 고용량의 스테로이드 및 면역억제제 투여나 방사선 치료, 수술 등을 했지만 근본적인 치료법은 없어 미충족 수요가 큰 질환으로 꼽혔다.
테페자는 자가항체와 IGF1R과의 결합을 차단하는 기전으로 개발됐다. 희귀의약품 지정을 통해 2020년 1월 미국 식품의약국(FDA)으로부터 최초의 갑상선안병증 치료제로 승인받았다. 이후 현재까지 FDA의 문턱을 넘은 갑상선안병증 치료제는 없다.
한올바이오파마는 현재 미국 협력사인 이뮤노반트를 통해 자가면역질환 치료제 후보물질(HL161)을 갑상선안병증 치료제로 개발하고 있다. 테페자가 IV 제형으로만 FDA의 허가를 받은 만큼, 한올바이오파마는 HL161이 SC제형이라는 점에서 강점이 있을 것으로 기대해왔다.
이번 계약에 따라 테페자 역시 SC제형의 갑상선안병증 치료제 경쟁에 뛰어들게 됐다. 제리스는 회사의 SC제형 변환 플랫폼 기술인 '제리젝트'로 SC제형의 테페자를 개발한다. 개발이 완료되면 호라이즌은 이 기술을 이전받을 수 있는 우선권(옵션)을 갖는다. 이후 제리스는 테페자SC 판매에 따른 기술사용료(로열티)를 수령할 수 있다. 그 외의 자세한 계약 조건은 공개되지 않았다.
시장조사기관인 리서치앤드마켓은 2020년 세계 갑상선안병증 환자를 38만4000명으로 추산했다. 2029년 43만8000명으로 증가할 것으로 전망했다.
호라이즌은 작년 1월 테페자의 미국 출시 후 이 약으로 16억6130만달러(약 2조2000억원)의 매출을 올렸다. 올 3분기 누적 매출도 14억7200만달러(약 1조9700억원)로 지난해 같은 기간의 10억7100만달러(약 1조4300억원)를 뛰어넘었다. 크리스 스캇 JP모간 바이오 담당 애널리스트는 최근 “호라이즌이 테페자만으로 연간 최대 40억달러(약 5조3500억원)의 매출을 낼 수 있을 것”이라고 분석했다.
그러나 테페자 관련 청력 손실 부작용이 보고되고 있어 한계로 지적된다. 최근 테페자 처방 후 청력 손실을 겪은 환자들이 호라이즌을 상대로 잇따라 고소장을 제출하고 있다. 테페자는 허가 전 임상에서도 같은 부작용이 여러차례 관찰됐다.
한올바이오파마는 이뮤노반트를 통해 연내 HL161의 갑상선안병증 미국 임상 3상을 시작한다. 중국 협력사인 하버바이오메드 지난해 10월 갑상선안병증 중국 2상의 첫 환자 투약을 시작했다. HL161은 자가항체의 세포 공격을 막는 테페자와 달리, 자가항체를 몸 속에 축적시키는 'FcRn' 수용체를 억제해 자가항체를 없애는 기전으로 개발되고 있다.
이도희 기자 tuxi0123@hankyung.com



![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


