차백신연구소는 면역증강제 플랫폼 기술인 엘-팜포(L-pampo)와 리포-팜(Lipo-pam)을 활용해, 만성 B형간염 치료 및 예방 백신, 대상포진 예방 및 치료 백신 등을 개발하고 있다. 항암백신으로도 개발을 확장하고 있다.
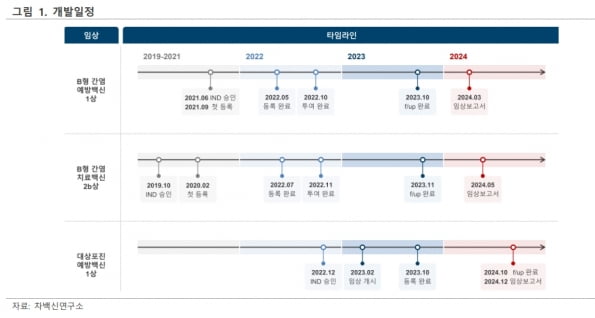
만성 B형간염 치료백신(CVI-HBV-002)은 현재 국내 임상 2상의 환자 투약을 마친 상태다. 차백신연구소는 3세대 B형간염 항원(L-HBsAg)을 개발하고, 여기에 면역증강제 엘-팜포 플랫폼을 접목했다. 앞서 1·2a상(투여 4주, 투여 2년 후 관찰)에서는 T세포 활성화와 만성 B형간염 표면항원(HBsAg) 감소 등 의미 있는 결과가 확인됐다.
2019년 12월부터 2b상을 진행 중으로, 지난해 11월 환자 153명에 대한 투약을 마쳤다. 1년 간의 관찰 및 통계분석을 거쳐 올해 말 임상을 마칠 예정이다. 2b상 결과는 내년 5월께 발표될 것으로 전망했다. 하태기 연구원은 “1·2a상에서 확인한 의미 있는 데이터가 2b상에서 그대로 확인된다면, 기술이전에 긍정적일 것”이라고 말했다.
기존 B형간염 백신으로는 대안이 없는 성인 무반응자용 B형간염 예방백신(CVI-HBV-002)에 대한 기대도 크다고 했다. B형간염 백신 무반응자는 전체 인구의 5~10%다.
차백신연구소는 2021년 7월에 국내 1상을 승인받아, 2022년 10월 말까지 피험자 전체 30명에 대해 투여를 완료했다. 투여 후 1년 간 관찰 및 통계분석을 연말까지 마무리하고, 내년 2상에 진입할 계획이다.
1상 중간결과에 대한 발표 없이 최종 결과보고서를 올해 말이나 내년 초에 발표할 것으로 봤다. 하 연구원은 “임상에서는 투여 후 모든 피험자에서 항체가가 매우 높이 올라가는 효과를 확인한 것으로 알려졌다”며 “2상은 환자가 많은 중국에서 진행할 가능성이 높아, 향후 중국과 동유럽으로의 기술이전이 추진될 수도 있다”고 했다.
리포-팜 플랫폼을 이용한 대상포진 예방백신(CVI-VZV-001)은 GSK의 ‘싱그릭스’ 대비 통증이 적다는 장점이 있다고 전했다. 2022년 12월 국내 1상을 승인받았다. 이달부터 3개월 동안 피험자 32명에 대한 투여를 진행하고, 1년 관찰을 진행할 예정이다.
하 연구원은 “1상 결과에 따라 내년 하반기에는 글로벌 빅파마와 공동임상이나 기술이전을 추진할 것”이라며 “예방백신 1상이 끝나면 이후 환자에 투여하는 치료개념 백신에 대한 1·2상도 추진한다는 계획”이라고 말했다.