에스티큐브, AACR서 넬마스토바트 1상 결과 포스터 발표
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
최대 투여량서 안전성 확인
추가 투여군 유효성 분석 중
추가 투여군 유효성 분석 중
에스티큐브는 미국암연구학회(AACR)에서 항암 후보물질 ‘넬마스토바트’의 글로벌 임상 1상 연구 결과를 포스터로 발표했다고 19일 밝혔다.
넬마스토바트는 에스티큐브가 발견한 면역관문 단백질 BTN1A1을 표적하는 면역항암제 후보물질이다. 연초 임상 1상을 마쳤다.
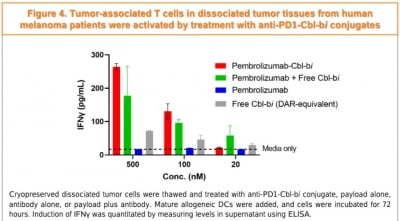
에스티큐브는 환자 혈액에서 넬마스토바트의 농도 및 사이토카인 발현, 면역세포 농도 변화 등을 측정했다. 암조직에서 PD-L1 종양비율점수(TPS), 복합양성점수(CPS), BTN1A1 발현 점수 등도 분석했다.
연구 결과 최대 투여량인 체중 1kg당 15mg까지 안전성을 확인했다. 현재 10mg 및 15mg의 추가 투여군(backfill cohort)에 대한 유효성을 관찰하고 있다.
에스티큐브는 이번 AACR에서 넬마스토바트 임상 1상에서 확인된 약동학 및 약력학적 특성 및 BTN1A1 발현 관련 진단용 항체 등에 대해서도 발표했다.
에스티큐브 관계자는 “BTN1A1이 기존 면역항암제 바이오마커인 PD-1, PD-L1과 상호 배타적인 새로운 면역관문이라는 것을 이번 임상근거로 또한번 확인했다”며 “PD-1, PD-L1 항체에 불응하는 경우 넬마스토바트는 혁신적 치료대안이 될 것”이라고 말했다.
박인혁 기자 hyuk@hankyung.com
넬마스토바트는 에스티큐브가 발견한 면역관문 단백질 BTN1A1을 표적하는 면역항암제 후보물질이다. 연초 임상 1상을 마쳤다.
에스티큐브는 환자 혈액에서 넬마스토바트의 농도 및 사이토카인 발현, 면역세포 농도 변화 등을 측정했다. 암조직에서 PD-L1 종양비율점수(TPS), 복합양성점수(CPS), BTN1A1 발현 점수 등도 분석했다.
연구 결과 최대 투여량인 체중 1kg당 15mg까지 안전성을 확인했다. 현재 10mg 및 15mg의 추가 투여군(backfill cohort)에 대한 유효성을 관찰하고 있다.
에스티큐브는 이번 AACR에서 넬마스토바트 임상 1상에서 확인된 약동학 및 약력학적 특성 및 BTN1A1 발현 관련 진단용 항체 등에 대해서도 발표했다.
에스티큐브 관계자는 “BTN1A1이 기존 면역항암제 바이오마커인 PD-1, PD-L1과 상호 배타적인 새로운 면역관문이라는 것을 이번 임상근거로 또한번 확인했다”며 “PD-1, PD-L1 항체에 불응하는 경우 넬마스토바트는 혁신적 치료대안이 될 것”이라고 말했다.
박인혁 기자 hyuk@hankyung.com


![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


