삼진제약, 웨어러블 심전도기 '에스패치EX' 미국 FDA 승인
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
제품 신뢰도 향상 기대
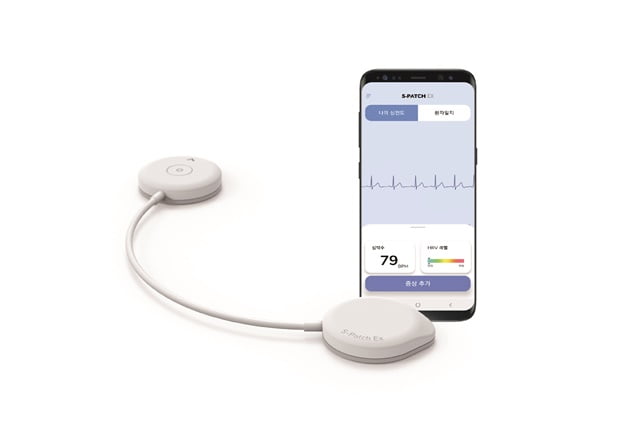
에스패치-EX는 2019년 삼성SDS로부터 분사(스핀오프)한 웰리시스가 개발 및 제조한 웨어러블 심전도 솔루션이다. 삼진제약은 국내 판매를 맡고 있다.
이 제품은 두께 6mm, 무게 9g의 작고 가벼운 크기로 IP55 등급의 방수·방진 기능을 갖췄따. 부정맥 및 심장질환 진단을 돕는 역할을 한다. 기존 홀터 심전도계의 불편함을 해소했다. 모바일 애플리케이션과 기기에서 사용자의 증상 기록이 가능하고, 기록된 증상이 자동으로 소프트웨어에 표시된다.
또 검사 종료 후 클라우드 서버로 데이터가 자동 전송돼 시간적, 물리적 제한 없는 판독이 가능하다. 이를 통해 환자는 병원 방문 횟수를 진료 상황에 맞게 적절히 조절할 수 있고, 의료진은 진료 일정 관리에도 도움을 받을 수 있다.
에스패치-EX는 국내 식품의약품안전처 허가와 함께 유럽 인증(CE), 호주 의약품허가처(TGA), 뉴질랜드 의약품의료기기안전청(MEDSAFE)에 의료기기 등록을 완료했다. 현재 전 세계 14개국에 제품을 제공하고 있다.
삼진제약은 에스패치-EX의 미국 FDA 승인으로 기술력과 안전성을 입증받아 향후 제품 신뢰도 향상 및 국내 시장 점유율 상승에 긍정적인 영향을 미칠 것으로 기대하고 있다.
삼진제약 헬스케어팀 관계자는 “에스패치-EX의 미 FDA 승인은 웨어러블 심전도 검사 시장 중 최대 규모로 평가받는 미국에서 제품의 안전성과 유효성을 인정받았다는데 큰 의미가 있다”며 “앞으로도 에스패치-EX를 통해 환자들의 부정맥 조기 진단뿐만 아니라 일반인의 건강검진 서비스, 심장질환 퇴원 환자의 사후 관리 등 활용 가능한 분야 발굴에 적극적으로 나설 것”이라고 말했다.
김예나 기자 yena@hankyung.com




![K팝 업계에도 '친환경' 바람…폐기물 되는 앨범은 '골칫거리' [연계소문]](https://img.hankyung.com/photo/202206/99.27464274.3.jpg)


