서울대병원 "염증 유발 리지스틴, 당뇨병 유발 규명"
-
기사 스크랩
-
공유
-
댓글
-
클린뷰
-
프린트
![[사진 왼쪽부터] 순환기내과 김효수·양한모 교수, 김준오 연구교수](https://img.hankyung.com/photo/202404/01.36427453.1.jpg)
김효수 서울대병원 순환기내과 교수팀(양한모 교수, 김준오 연구교수)은 세포분석을 통해 리지스틴 분비 기능과 CB1 수용체를 함께 보유한 인간 단핵구세포를 발견했다고 15일 발표했다. 연구팀은 인간화 동물모델을 통해 이 세포가 비만으로 인한 당뇨병 발병에 핵심 역할을 한다는 사실을 입증했다.
리지스틴은 인간 단핵구에서 분비되는 사이토카인이다. 만성염증을 유발하는 것으로 알려졌다. 그동안 마우스 모델에선 리지스틴이 지방세포에서 분비돼 비만으로 인한 당뇨병을 유발한다고 보고됐다. 이전 연구에선 이 물질과 인간 당뇨병 발병 간의 인과관계는 알려지지 않았다.
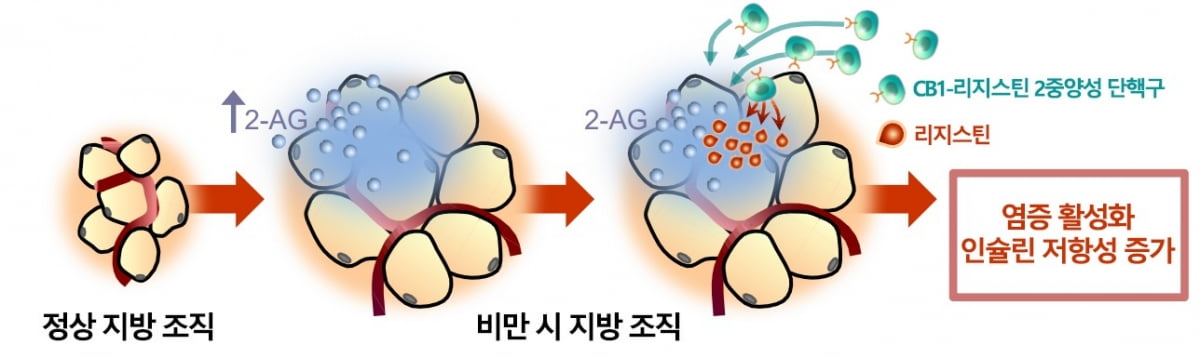
ECS는 신경전달물질인 엔도카나비노이드(2-AG)와 CB1 수용체가 결합해 행복감, 식욕증진 등을 유도하는 시스템이다. 규칙적인 운동을 한 뒤 뇌에서 엔도카나비노이드가 분비돼 이 시스템이 활성화되면 만족감을 느끼고 식욕이 올라가는 기전이 작동한다.
이런 시스템을 자극하는 또 다른 물질은 마리화나다. 이를 흡인하면 행복감과 식욕이 증가하는 데 이런 기전이 작동하기 때문이다.
이번 연구도 엔도카나비노이드 체계가 비만 당뇨병 등 대사질환 발병에 기여한다는 데에 초점을 맞추고 진행됐다.
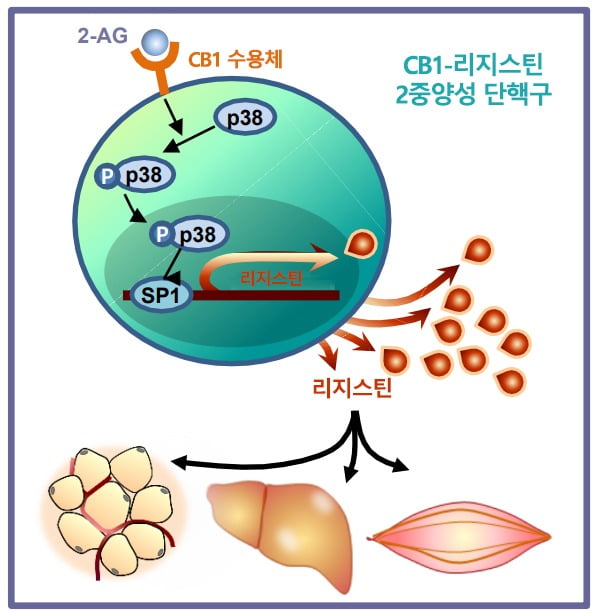
연구팀은 인간화 마우스 모델을 활용해 이 단핵구가 실제 인간 당뇨병 발병에 미치는 영향을 검증했다. 골수 이식을 거쳐 인간 단핵구를 보유하게 된 생쥐와 인간 리지스틴이 발현되도록 유전자를 조작한 생쥐를 대상으로 8주간 고칼로리 음식을 투여한 뒤 근육·간·지방조직에 2-AG 수준,CB1 농도, 리지스틴 농도, 인슐린 작용 등을 측정했다.
그 결과 고칼로리 식이를 섭취한 인간화 생쥐는 근육·간·지방 조직의 2-AG 양이 증가했다. 이 때문에 리지스틴이 분비됐고 미토콘드리아 구조가 파괴되고 기능이 떨어졌다. 인슐린 효과가 떨어지는 인슐린 저항성으로 이어졌다.
연구팀은 엔도카나비노이드 시스템과 연결된 2중-양성 단핵구세포가 말초혈액을 순환하다가 2-AG가 많이 쌓인 목표 장기에 침투해 리지스틴을 분비하고 미토콘드리아를 파괴해 인슐린 저항성과 당뇨병을 유발한다는 것을 증명했다고 설명했다.
이번 연구를 통해 엔도카나비노이드 수용체 차단제(SR141716)를 투여해 2-AG와 CB1 수용체 결합을 차단한 생쥐는 고칼로리 음식을 먹인 뒤에도 인슐린 저항성이 높아지지 않았다. 'SR141716' 투여 후엔 고칼로리 식이 탓에 증가한 2중-양성 단핵구 침투가 차단됐다. 그 결과 지방조직에서 리지스틴 농도가 낮아지고 염증이 가라앉았다.
연구팀은 이런 연구 결과가 인슐린 저항성을 조절하고 당뇨병을 예방하는 새 치료제 개발 가능성을 보여준다고 설명했다. 연구팀은 리지스틴과 그 수용체인 캡1 단백질 상호결합을 억제하는 리지스틴 차단 항체를 개발했다. 이를 바탕으로 대사질환·염증성장질환 등의 새 치료제를 개발하고 했다.
김 교수는 "사람의 말초혈액을 순환하는 단핵구의 20%는 CB1-리지스틴 2중-양성 세포"라며 "해당 세포가 비만해졌을 때 대사질환을 야기하는 핵심 행동대원임을 연구를 통해 발견했다"고 했다. 그는 "엔도카나비노이드 수용체를 차단해 비만에 의한 당뇨병을 예방하는 새 치료제 개발 가능성을 타진할 수 있었다"고 했다.
이번 연구는 보건복지부 연구중심병원 프로젝트 지원을 받아 진행됐다. 사이언스 자매지인 '리서치' 온라인판에 실렸다.
이지현 기자 bluesky@hankyung.com



