키트루다의 지난해 매출은 약 140억 달러. 오는 2026년엔 250억 달러까지 늘어날 전망이다. MSD의 지난해 전체 매출 480억 달러(추정치) 중 약 30%는 키트루다에서 나왔다. 하지만 현세대 면역항암제는 그 한계점이 명확하다. 절반에 한참 못 미치는 낮은 반응률을 해결해야만 한다. 약이 일단 듣기만 하면 완치가 가능하다는 말이 나올 만큼 효과가 좋지만, 그렇지 않은 환자에겐 사실상 무용지물이다.
반응률은 암종에 따라 다르지만, 일반적으로 20~30% 정도다. 삼중음성유방암에서의 반응률은 약 5%, 대장암과 췌장암에서는 거의 듣지 않는 것으로 알려져 있다. ‘암이 완치되거나 아니면 효과가 없거나…’. 이 동전의 양면과도 같은 반응률을 높이기 위해 세계 제약·바이오 업체들이 대거 뛰어들었다.
면역항암제, 그 반쪽의 성공
첫 면역항암제는 2011년 미국 식품의약국(FDA)의 승인을 받아 출시된 여보이(BMS)다. 여보이는 T세포의 활동을 억제하는 CTLA-4 수용체를 타깃으로 하는 항체로 개발됐다. 암세포는 자신을 지키기 위해 접근하는 면역세포를 불활성화할 수 있는 물질(리간드)을 분비하는 데 이런 물질 중 하나가 달라붙는 곳이 바로 T세포의 CTLA-4 수용체였다. 여보이는 T세포의 CTLA-4 수용체에 한발 먼저 달라붙어 암세포가 분비한 물질이 붙는 것을 차단한다. 암세포가 벌이는 일련의 연쇄적인 면역세포 회피 프로세스를 사전에 차단하는 식으로 작동한다. 그러나 여보이는 면역항암제의 맏형이었음에도 시장의 승자가 되지 못했다.
특히 T세포를 임의로 활성화하면서 발생하는 자가면역질환 등의 부작용 측면에서 PD-1 계열 면역관문억제제가 CTLA-4 계열에 비해 더 적었다. CTLA-4는 T세포가 항원제시세포를 만나 활성화되는 초기 단계에 전방위로 작용하는 반면, PD-1은 T세포가 암세포를 공격하는 최종 단계에 작용한다는 점도 임상 결과에 영향을 준 것으로 평가된다.
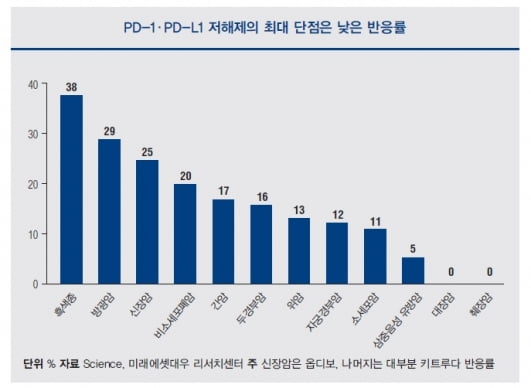
반면 면역관문억제제의 한계점도 명확하게 드러났다. 흑색종을 비롯해 호지킨림프종, 메르켈 세포암, 현미부수체 불안정 암 등에서는 50%를 넘는 반응률이 나오지만, 그 외의 적응증에서는 반응률이 15~25%로 떨어졌다. 원인으론 암세포가 PD-1 면역관문 외에도 다양한 면역 회피 기전을 갖고 있기 때문으로 밝혀졌다. 즉 면역관문억제제가 막지 못하는 또 다른 면역 회피 기전을 통해 T세포의 활성이 억제되면 암세포가 살 수 있기 때문이다. 현재 진행 중인 병용요법은 면역관문억제제의 한계점을 보완하기 위한 방향으로 시도되고 있다.
병용요법 임상 2900건
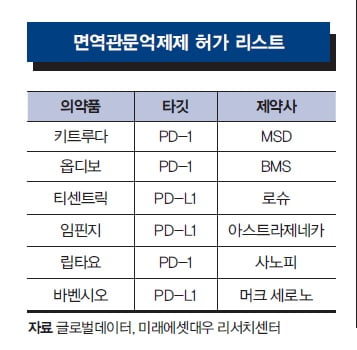
면역관문억제제는 표적하는 면역관문에 따라 분류할 수 있다. 앞서 설명했듯 여보이는 CTLA-4를, 키트루다와 옵디보는 PD-1을 타깃으로 한다. 티센트릭(로슈)과 임핀지(아스트라제네카)의 표적은 PD-1 수용체와 결합하는 리간드인 PD-L1이다. 지금까지의 결과에서는 PD-1 계열 면역관문억제제가 가장 앞선다. 병용요법 임상시험 또한 이 같은 시장의 논리에 따라 진행되고 있다.
지난해 11월 미국 암연구원(CRI)의 연례 발표에 따르면 지난해 9월까지 등록된 PD-1 및 PD-L1 계열 면역관문억제제의 임상시험은 총 4400건이다. 이 중 단일요법을 제외한 병용요법 임상 건수는 2900건이다.
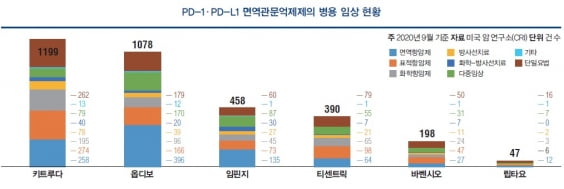
허가된 6종의 PD-1 및 PD-L1 면역관문억제제별 임상 건수를 보면 대다수가 시장 1위인 키트루다와 2위 옵디보와의 병용요법에 집중됐다. 병용 치료 임상 건수는 키트루다 937건, 옵디보 899건으로 병용요법 전체 임상 수의 63.3%를 차지했다. PD-L1 저해제 임핀지와 티센트릭은 각각 398건, 311건에 그쳤다.
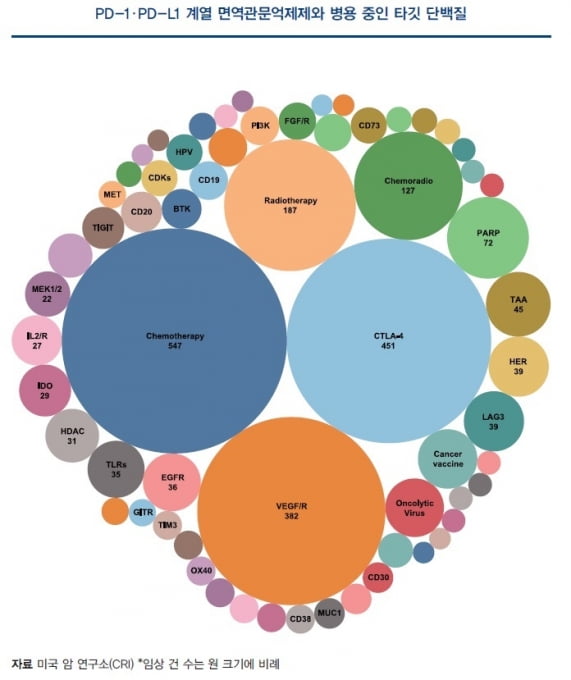
PD-1, PD-L1 계열 면역관문억제제와 함께 선택되는 치료법으로는 다른 면역항암제와의 병용이 892건으로 가장 많았다. 이어 2세대 항암제인 표적항암제와의 병용이 664건이었으며, 2개 이상의 치료법이 함께 선택되는 다중임상(multi-way-combo)은 429건이었다. 또 1세대 항암제인 화학항암제와의 병용이 428건이었으며 방사선치료와의 병용이 178건이었다.
3년 전인 2017년과 지난해 기록을 비교하면 면역관문억제제와 조합하는 방법의 종류가 크게 증가한 점도 눈에 띈다. CTLA-4와 IDO 저해제를 비롯해 124종류였던 조합(타깃) 대상이 지난해 들어 253종으로 늘어났다.
가장 많은 임상이 진행된 병용요법으론 화학항암제와의 조합이 547건으로 가장 많았다. 이어 여보이 등 CTLA-4 계열 면역관문억제제와의 병용요법이 451건, 혈관내피세포성장인자(VEGF) 또는 혈관내피세포성장인자 수용체(VEGF R)를 타깃으로 한 병용요법이 382건으로 뒤를 이었다.
특히 VEGF 또는 VEGF R을 타깃으로 한 병용요법은 2017년과 비교해 임상 건수가 가장 급격하게 늘어난 병용 방식으로 꼽혔다. 57건에서 382건으로 6배 이상 늘었다. 로슈의 PD-L1 저해제 티센트릭과 아바스틴의 병용요법이 대표적이다.
지난해 5월 FDA는 이전에 전신 치료를 받지 않은 절제 불가능한 간세포암 1차 치료단계에서 쓸 수 있도록 승인했다. 티센트릭과 아바스틴 병용요법은 임상 3상에서 기존 간암 치료제인 바이엘의 넥사바와 비교해 질병 악화 또는 사망 위험을 40% 이상 감소시킨 것으로 나타났다. 종양미세환경은 면역관문억제제의 활성을 저해하는 요인으로 꼽히는데, 종양미세환경을 구축하는 데 핵심적인 역할을 하는 신생혈관이 형성되지 못하도록 하는 전략을 취한 것으로 풀이할 수 있다.
VEGF에 이어 가장 많은 임상이 시도된 조합으론 브라카1(BRCA1)과 브라카2(BRCA2) 유전자의 돌연변이가 있는 난소암과 유방암 치료에 쓰이는 PARP 저해제가 꼽혔다. 지난해 9월 기준 72건의 병용 임상시험이 진행 중이다. PARP 단백질은 DNA 복제 시 발생하는 오류를 복구하는 역할을 하는 단백질이다. PARP 단백질의 활동을 저해할 경우 정상세포보다는 암세포에서 높은 세포 독성이 나타난다. DNA 복제 시 발생하는 오류를 수정할 수 있는 다양한 기전을 가진 일반 세포와 달리 암세포는 그렇지 못해 사멸하게 되는 원리를 이용한 것이다. PARP 저해제로는 클로비스 온콜로지의 루브라카, 아스트라제네카의 린파자가 유명하다.
PD-1 및 PD-L1 계열 면역관문억제제와 LAG-3 저해제의 병용임상은 39건이 등록됐다. T세포와 B세포, NK세포 등에서 발현하는 LAG-3는 PD-1처럼 T세포의 활성화와 사이토카인을 억제하는 역할을 한다. 이런 특징 때문에 단독 요법도 진행된 적이 있으나 PD-1과 달리 효과가 미미했다. 하지만 이뮤텝의 LAG-3 저해제 IMP321이 키트루다와 함께 병용 투여했을 때 키트루다의 반응률을 높이는 임상 결과가 나와 기대가 커지고 있다. 비소세포폐암 1차 치료제로서 키트루다와 병용했을 때 환자 17명에게서 객관적 반응률 52.9%라는 수치를 얻을 수 있었다. 키트루다 단독의 경우 객관적 반응률이 20%, 여보이와 옵디보 병용요법이 33%였던 것에 비해 2.5배 이상 높다.

사이토카인은 병용요법의 등장 덕분에 재조명되고 있다. 사이토카인은 과거 단독 투여 약물로 허가됐다가 전신 면역반응을 과도하게 유도하는 부작용과 함께 체내에서 활성을 장기간 유지하기 어렵다는 문제점 때문에 현재는 단독으로 잘 쓰이지 않았다.
제넥신과 네오이뮨텍이 공동개발 중인 ‘하이루킨’은 면역세포인 B세포와 T세포의 발달에 핵심역할을 하는 사이토카인 인터류킨-7(IL-7)에 기반한 면역항암제 후보물질이다. IL-7의 짧은 반감기 문제를 제넥신이 기술적으로 해결하면서 삼중음성유방암을 적응증으로 한 키트루다와의 병용 임상을 진행하고 있다. IL-7과의 병용요법 임상은 지난해 5건이 등록됐다. 이 외에도 지난해 IL-1을 이용한 병용 임상은 6건, IL-2는 27건, IL-12는 8건, IL-15은 9건이 등록됐다.
*이 기사는 <한경바이오인사이트> 매거진 2021년 1월호에 실렸습니다.









