오칼리바는 담즙성 담관염 치료제로 FDA 승인을 받았던 약이다. 담즙성 담관염이란 담즙이 제대로 분비되지 못하고 장기 내에 갇혀 염증과 섬유화를 일으키는 질환이다. 오칼리바는 간과 장에서 발현하는 파네소이드 X 수용체(FXR)를 표적으로 삼아 염증과 섬유화와 관련한 대사경로를 조절하는 식으로 작동한다. 인터셉트는 임상 3상에서 오칼리바가 NASH의 악화를 막고 섬유증을 감소시킨다는 결과를 얻었다.
하지만 FDA의 판단은 달랐다. NASH 환자에게 오칼리바를 투여했을 때 얻는 이익이 부작용으로 인한 손실보다 크지 않다고 봤다. 오칼리바는 유해한 콜레스테롤을 증가시켜 심혈관계 위험을 높이는 등의 부작용이 있다. 게다가 NASH 환자들은 이미 과체중이거나 제2형 당뇨를 앓는 등 기저질환이 있는 만큼 오칼리바의 부작용이 NASH 환자들에게 더 위협적일 수 있다고 FDA가 판단한 것이다.
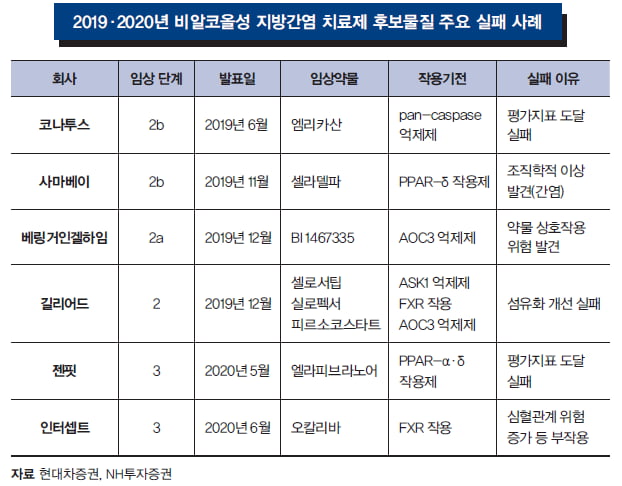
2019·2020년은 ‘잔인한 해’… 임상 실패 잇따라
2019년은 베링거인겔하임, 길리어드 등 NASH 치료제 개발에 뛰어든 글로벌 제약사들이 무더기로 고배를 마신 해였다.
베링거인겔하임의 NASH 후보물질 ‘BI 1467335’는 2015년 오스트레일리아 제약사 파막시스에서 도입했다. BI 1467335는 AOC3을 표적으로 하는 NASH 치료 후보물질이다. AOC3은 면역세포를 자극하고 염증 반응을 일으켜 섬유화에 이르게 하는 기전에 관여하는 것으로 알려져 있다.
BI 1467335는 이 AOC3을 억제해 NASH 환자에게서 발생한 섬유화 진행을 막고 나아가 이를 개선하는 효과까지 기대할 수 있는 약물로 주목받았다. 2019년 12월 베링거인겔 하임 측은 “임상 2a상에선 긍정적인 결과를 얻었으나 약물 상호작용에서 위험 요소를 발견하고 개발을 중단하게 됐다”고 설명했다.
길리어드는 2019년 12월 임상 2상을 진행 중이던 다수의 NASH 파이프라인 개발을 중단했다. 길리어드가 단독 또는 병용 임상을 진행 중이던 파이프라인은 ASK1 억제제 ‘셀로서팁’, FXR 작용제 ‘실로펙서’, AOC3 억제제 ‘피르소코스타트’ 등이다.
실로펙서는 인터셉트의 오칼리바와 피르소코스타트는 베링거인겔하임의 BI 1467335와 표적이 유사한 파이프라인이다. 셀로서팁은 AS인데, ASK1은 면역세포를 활성화해 염증반응을 일으키고 나아가 섬유화를 유발하는 효소다. 하지만 길리어드는 끝내 이들 3가지 후보물질의 단독 및 병용 임상이 실패했다고 했다. 임상에서 섬유화를 개선하는 효과가 미미했기 때문이라고 길리어드는 밝혔다.
미국 제약사 시마베이 또한 2019년 11월 임상 2b상까지 진행한 후보물질 ‘셀라델파’의 임상시험 중단을 발표했다. 중단 사유는 비 전형적 간 손상이다. 셀라델파는 이상지질혈증(atherogenic dyslipidemia)을 개선하는 효과가 있는 것으로 알려진 PPAR-δ 작용제다.
앞선 동물실험에서는 독성 지질 등을 분해하고 간 수준을 정상으로 되돌리는 기능을 확인했으나 사람을 대상으로 한 실험에선 간염 등의 부작용이 나타났다.
지난해엔 젠핏의 NASH 치료제 후보물질 ‘엘라피브라노어’도 임상 3상에서 고배를 마셨다. 엘라피브라노어는 시마베이의 셀라델파가 표적으로 삼았던 PPAR-δ뿐 아니라 PPAR-α까지 동시에 표적으로 하는 이중작용제로 설계됐다.
PPAR-α는 PPAR-δ와 마찬가지로 심혈관계 질환 및 이상지질혈증 개선을 목적으로 하는 치료제 개발에서 주목받는 표적 중 하나다. 실패 사유는 위약군과 대조했을 때 통계적으로 유의미한 효과를 보지 못했다는 것이다.
의미 없는 실패 없다, 바통 넘겨받는 새 파이프라인들
LG화학은 지난해 NASH 치료제인 ‘TT- 01025’의 미국 임상 1상을 승인받았다. 중국 트랜스테라 바이오사이언스로부터 도입한 TT-01025는 VAP-1 저해제로, AOC3 저해제와 사실상 표적이 같다. 후기 임상에서 좌초된 베링거인겔하임의 BI 1467335와 길리어드의 피르소코스타트가 AOC3 저해제였다.
제약업계에서는 후기 임상에서 부작용과 저 조한 효능으로 개발이 중단되기도 했지만 여전히 가능성이 있는 표적으로 AOC3을 지목했다. 여러 제약사에서 임상 1상을 거친 만큼 기본적으로 약물의 안전성이 입증돼 부작용과 효능 미미 사이의 절충점만 찾을 수 있다면 여전히 길은 열려 있다고 보기 때문이다.
최근에는 GLP-1과 FGF21이 새롭게 주목받고 있다. GLP-1은 펩타이드 호르몬으로 인슐린 분비를 강화해 혈당 수치와 체중을 낮추는 효과가 있다. 비만 치료제로 유명한 ‘삭센다’의 주성분이 바로 이 GLP-1이다. 대사를 증가시키고 체중을 낮추면 지방간 수치가 낮아지는 효과를 노렸다. 삭센다로 널리 쓰였기 때문에 안전성에 대한 부담이 적은 것도 장점이다.
FGF21은 섬유아세포 성장인자로 체내에서 염증을 억제하는 역할을 한다. 간의 섬유화는 염증 반응의 결과로 나타나기 때문에 염증 반응을 억제하면 섬유화 진행을 막을 수 있다.
삭센다 개발사인 노보노디스크가 GLP-1을 이용한 파이프라인의 임상 2상을 진행 중이며, 미국 바이오벤처 아케로 테라퓨틱스는 FGF21 억제제에 기반한 파이프라인의 임상 2상을 하고 있다.
국내에선 유한양행이 GLP-1과 FGF21을 모두 타깃으로 하는 2중 작용제를 베링거인겔하임과 함께 개발하고 있다. 한미약품은 GLP-1을 GIP, 글루카곤과 병합한 3중 작용제의 임상시험을 진행하고 있다.
*이 기사는 <한경바이오인사이트> 매거진 2021년 5월호에 실렸습니다.