지씨셀·엔케이맥스 등
NK세포치료제 美임상 돌입
큐로셀·앱클론·티카로스는
국내서 CAR-T 치료제 임상

미국 임상에 나선 국내 기업들
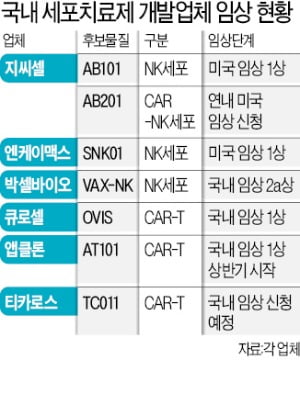
AB201은 보통 T세포에만 붙이던 암세포를 추적하는 역할을 하는 키메릭항원수용체(CAR)를 붙인 NK세포 치료제다. 흔히 ‘CAR-NK’라고 부르며, 세포치료제 중에서도 신기술로 꼽힌다. AB201은 암 중에서도 유방암 환자에게서 자주 발견되는 수용체(HER2)를 찾아 유도탄처럼 공격하도록 설계됐다. 지난해 3월 미국에서 투약을 시작한 NK세포 치료제 ‘AB101’의 임상 1상 성적표는 올해 중 공개한다. 지씨셀은 기존 요법이 듣지 않는 비호지킨 림프종 환자에게 AB101을 표적항암제 리툭시맙과 함께 투약하고 있다.
엔케이맥스는 육종암 환자를 대상으로 미국에서 진행한 임상 1상 결과를 오는 6월 열리는 미국 임상종양학회(ASCO)에서 발표한다는 계획이다. 엔케이맥스는 NK세포 치료제(SNK01)와 면역관문 억제제(바벤시오, 키트루다)의 병용 임상을 하고 있다. 차기 임상도 계획대로 진행되고 있다. 엔케이맥스 관계자는 “아피메드와 공동으로 하는 미국 임상 또한 1분기 첫 투약을 시작할 예정”이라고 말했다.
국내에선 CAR-T 임상 릴레이
국내에서는 암세포만 쫓도록 유전자를 조작한 CAR-T 치료제 임상 바람이 불고 있다. 선두주자는 큐로셀이다. 환자 10명에게 투약한 임상 1상 결과를 ASCO에서 발표한다는 계획이다. 임상 2상은 오는 3월부터 시작하기로 했다. 총 65명에게 투약하는 것이 목표다.지난달 식품의약품안전처로부터 CAR-T 치료제 ‘AT-101’에 대한 임상시험계획을 승인받은 앱클론은 상반기 첫 환자에게 CAR-T 치료제를 투약할 예정이다. 티카로스는 2~3월께 CAR-T 치료제 ‘TC011’의 임상시험계획을 식약처에 제출한다.
국내 세포치료제 업체들이 넘어야 할 ‘허들’은 이미 시판 중인 세포치료제를 뛰어넘는 일이다. 회당 치료 비용이 5억원에 이르는 CAR-T 치료제 ‘킴리아’는 국내 건강보험 적용을 앞두고 있다. 국내 신약 벤처들은 치료할 암 종류(적응증)를 달리하거나 경제성을 높이는 방향으로 경쟁력을 키우고 있다. 엔케이맥스가 도전 중인 육종암은 기존 항암제나 세포치료제가 듣지 않는 분야다. 지씨셀의 AB101이 도전 중인 비호지킨 림프종은 기존 CAR-T와 경쟁해야 하는 암종이지만 환자 맞춤형이 아니라 누구나 쓸 수 있는 범용 제품으로 개발하고 있다. 환자 맞춤형인 기존 CAR-T 치료제에 비해 가격 면에서 우위를 점할 수 있다는 전망이 나온다.
이우상 기자 idol@hankyung.com