과학과 놀자 (44) 화학반응에 대한 이해

반응속도는 가장 느린 과정에 의해 결정
화학반응은 어떠한 물질이 화학 변화를 겪어 다른 물질로 변화하는 과정이다. 화학반응의 중요한 두 요소는 ‘반응속도’와 ‘화학평형’ 개념이다. 반응속도는 어떤 화학 반응이 일어나는 속도를 말한다. 예를 들어 공기 중에서 쇠가 산화되는(녹스는) 반응은 몇 년이 걸리는 느린 반응이지만, 부탄가스가 연소되는 반응은 단 몇 초 만에 일어난다. 이처럼 반응속도는 반응온도, 압력, 반응물·생성물 농도, 촉매 사용 여부에 따라 영향을 받는다.대부분 촉매는 반응속도를 증가시켜 주는 역할을 하며, 화학과와 화학공학과에서 다루는 촉매의 종류는 다르다. 화학과에서는 반응물과 촉매의 상(phase: 물질의 상태)이 같은 균일(homogeneous) 촉매를 다룬다. 즉 반응물과 촉매가 모두 액체기 때문에 반응물이 촉매에 접촉하는 현상을 크게 고려하지 않는다. 화학공학과에서는 반응 이후 반응물과 촉매를 쉽게 분리하기 위해 반응물과 촉매 간 상이 다른 불균일(heterogeneous) 촉매를 사용한다. 일반적으로 반응물의 상은 액체, 기체 또는 액체/기체며 촉매는 주로 고체를 사용한다.
반응물이 촉매 활성점에 도달하는 과정(확산, 흡착)과 촉매 표면반응 중 더 느린 과정이 ‘속도 결정단계’며, 이는 전체 반응시간을 결정한다. 대전 유성구에 있는 한국에너지기술연구원에서 부산역을 간다고 가정하면, 연구원에서 대전역까지 택시로 20분이며 부산역까지는 KTX로 2시간이 걸린다. 여기서 속도 결정단계는 KTX 타고 가는 과정이며 전체 시간은 KTX 시간에 의해 결정되는 것이다. 표면 반응속도가 속도 결정단계일 때 온도가 10℃ 증가할 때마다 반응속도가 2배 증가한다는 경험법칙이 있다(사실 특정 활성화 에너지와 온도에서만 성립). 만약 물질전달이 속도 결정단계일 경우 100℃를 증가시켜도 전체 반응속도는 고작 1.7% 정도만 증가할 수 있다. 어느 과정이 속도 결정단계인지 정확히 파악하고, 그 속도를 증가시킬 수 있는 변수를 적절히 조절해야 한다.
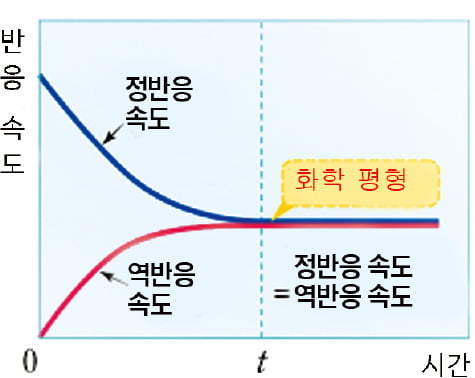
화학평형은 겉보기에 아무 변화가 없는 상태
화학평형은 반응의 종착지를 알려준다. 정반응 속도와 역반응 속도가 같아져 겉보기에 화학 반응이 일어나지 않는 것처럼 보이는 상태를 의미한다. 예를 들어 암모니아 합성 반응에서 암모니아가 생성(정반응)되는 속도와 암모니아가 수소와 질소로 분해(역반응)되는 속도가 같은 지점이 바로 화학평형 상태다. 마찬가지로 금속을 일정한 열량으로 가열한다면 충분한 시간 후에는 금속의 온도가 일정하게 유지되며 이 지점이 평형 상태라고 볼 수 있다. 금속의 온도를 증가시키는 요인(가열)과 감소시키는 요인(열 손실)이 발생하고 있지만, 그 정도가 같기 때문에 금속의 온도가 일정하게 유지되는 것이다. 바로 화학평형 지점에서 최대 전환율인 평형 전환율을 얻을 수 있다. 평형 전환율은 반응온도, 압력, 반응물 농도에 영향을 받는다. 촉매는 반응속도(평형에 도달하는 시간)에만 영향을 줄 뿐 종착지인 화학평형에는 영향을 주지 못한다.반응이 일어남에 따라 열이 흡수(흡열반응)되거나 발생(발열반응)하기도 한다. 식물은 물과 이산화탄소를 결합해 포도당과 산소를 만드는 광합성 반응을 하며 이 반응은 대표적인 흡열반응 중 하나다. 화학평형 측면에서 흡열반응은 열이 충분히 공급돼야 반응이 더 많이 일어날 수 있으며, 발열반응의 경우 열을 잘 제거해줘야 반응이 더 많이 일어난다. 열을 어떻게 공급 혹은 제거할 것인가는 반응기를 어떤 형태로 제작할 것인가에 영향을 준다. 그리고 심한 발열반응의 경우 안전을 위해 온도 제어가 필수적이다. 반응기를 설계하기 위해서 반응공학, 촉매공학, 유체역학, 물질전달, 열역학, 설계 기술 등 다양한 학문이 요구되며 검증을 위해선 실제 반응기와 비슷한 대규모 실험 장치가 필요하다.
화학 반응기 설계 기술은 아직 미흡
반응기를 설계하는 일은 종합적인 학문을 필요로 할 뿐만 아니라 시행착오(시간, 돈)가 많이 요구된다. 우리나라는 반응공정을 직접 설계하기보다 해외에서 기술을 구매해 빠른 속도로 산업화를 진행했다. 그로 인해 울산석유화학 단지가 조성된 지 벌써 50년이 지났지만, 아직도 반응기 설계기술은 미흡한 실정이다. 앞으로 빠른 추격자(fast follower)에서 미래 선도자(first mover)로 변모하기 위해서는 꾸준하고 우직한 노력이 필요할 것이다.√ 기억해주세요



!["근처 갈 만한 커피숍 알려줘"…'이 번호' 누르자 챗GPT가 받았다 [송영찬의 실밸포커스]](https://img.hankyung.com/photo/202412/01.38983952.3.jpg)






