“한미약품, 美 품목허가 일정 및 주요 임상 결과가 중요”
입력
수정
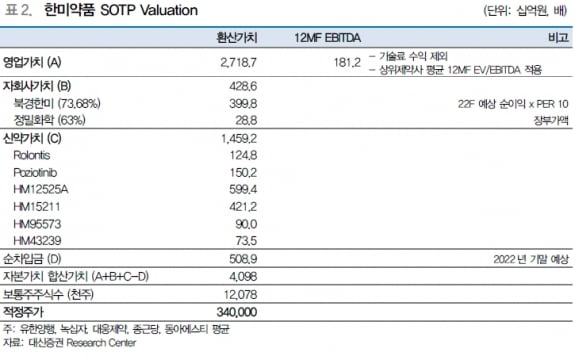
대신증권 분석
작년 4분기 매출과 영업이익은 각각 3189억원과 372억원으로 예상했다. 매출은 전년 동기 대비 15% 늘고 영업이익은 11.2% 줄어든 수치다. 앱토즈에 기술이전한 ‘HM43239' 관련 기술료 수익 인식과 북경한미의 실적 성장에 따라 시장 전망치(컨센서스)는 4%와 15% 웃돌 것이란 추정이다. 올해에는 신약후보물질에 대한 품목허가 승인 및 주요 임상 결과 발표가 예정돼 있다.
미국 협력사 스펙트럼은 지난해 12월 'HER2 Exon20' 삽입 변이가 있는 비소세포폐암(NSCLC)에 대해 포지오티닙의 신약허가를 FDA에 신청했다. 포지오티닙은 신속심사대상(패스트트랙)으로 지정돼 6개월의 심사를 받는다. 이르면 올 하반기 조건부허가 획득을 기대할 수 있다는 관측이다.
스펙트럼은 올 1분기 롤론티스에 대한 바이오의약품 품목허가신청서(BLA)를 재신청할 예정이다. 지난해 8월 최종보완요구서(CRL)를 수령한 후 자료를 보완 중이다. 연내 평택 바이오 공장에 대한 재실사를 받은 이후 내년 미국 출시가 기대된다는 설명이다. 2020년에 MSD에 기술수출한 ‘에피노페그듀타이드’는 비알콜성지방간염(NASH) 후보물질로, 임상 2a상 중간 결과를 연내 발표할 예정이다.
임윤진 연구원은 “‘랩스 트리플 아고니스트’도 연내 글로벌 임상 2상 중간 결과 발표가 기대된다”며 “긍정적인 결과가 확인될 경우, 기술이전 기회가 확대될 수 있을 것”이라고 말했다.
박인혁 기자